
下列反应中,硝酸既表现酸性,又表现氧化性的是( )。
A.Fe2O3跟稀硝酸反应 B.铜跟稀硝酸反应
C.CuO跟稀硝酸反应 D.Al(OH)3跟稀硝酸反应
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源:2016届福建省南平市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于铁及其化合物的说法正确的是
A、铁与CuSO4溶液反应后滴加KSCN溶液,溶液变红
B、FeCl2既有氧化性又有还原性
C、除去FeCl2溶液中的少量氯化铁,可通入氯气
D、补铁保健品中,含有+3价的铁元素
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省嘉峪关市高一上学期期中考试化学试卷(解析版) 题型:选择题
100mL0.3mol·L-1Na2SO4溶液和50mL0.2mol·L-1Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度(设体积为二者之和)为( )
A.0.2mol?L-1 B.0.25 mol?L-1 C.0.4 mol?L-1 D、0.5 mol?L-1
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省嘉峪关市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.能电离出H+的化合物叫做酸
B.能电离出OH-的化合物叫做碱
C.氧化物就是含有氧元素的化合物
D.化合物分为酸、碱、盐和氧化物是用树状分类法分类的
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高一上学期期末考试化学试卷(解析版) 题型:计算题
把1.0 mol·L-1 CuSO4和0.50 mol·L-1 H2SO4溶液等体积混合(假设混合后的溶液的体积等于混合前两种溶液的体积之和)计算:
(1)混合溶液中CuSO4和H2SO4的物质的量浓度c(CuSO4)=_______ c(H2SO4)=_________
(2)混合液中H+、SO42-的物质的量浓度c(H+)=__________ c(SO42-)=_________
(3)向溶液中加入铁粉,经过足够长的时间,铁粉有剩余。此时溶液中Fe2+的物质的量浓度c(Fe2+)=___________________________
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高一上学期期末考试化学试卷(解析版) 题型:选择题
下列试剂中,必须用橡胶塞的细口瓶贮存的是( )。
A.氢氟酸 B.氢氧化钠溶液 C.盐酸 D.氯化钠溶液
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高一上学期期末考试化学试卷(解析版) 题型:选择题
硅及其化合物在材料领域中应用广泛。下列叙述中,正确的是( )。
A.晶体硅是良好的半导体材料
B.硅是地壳中含量最多的元素
C.SiO2不溶于水,也不溶于任何酸
D.用带玻璃瓶塞的试剂瓶盛放NaOH溶液
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期末考试化学试卷(解析版) 题型:填空题
2016年奥运会将在里约热内卢举行,下图类似奥运五环,表示A、B、C、D、E五种化合物,环交叉部分代表两种化合物含有一种相同元素,且交叉部分所代表的的元素各不相同,五种化合物由五种短周期元素组成,且每种化合物仅由两种元素组成。A是可燃冰的主要成分;B、E分子中所含电子总数均与硅烷(SiH4)分子的电子数相等,B不稳定,具有较强氧化性,能发生自身氧化还原反应,E的相对分子质量为32,具有还原性,且常用作航天器的燃料;D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2。
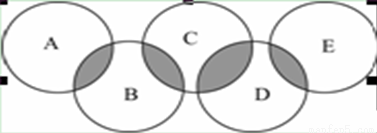
(1) D的化学式为________。
(2)A、B、E中含有一种相同的元素,其名称为________。
(3)B和E反应可生成一种单质和一种常见的液态化合物,写出化学方程式________。
(4)写出C与氢氧化钾溶液反应的离子方程式___________。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省高一上学期期中考试化学试卷(解析版) 题型:填空题
(1)已知将盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。 现有一个氧化还原反应的体系中共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
①该反应中,化合价升高的反应物是________,化合价没有发生变化的反应物是_______。
②写出一个包含上述七种物质的氧化还原反应方程式(不需配平) ___________。
③上述反应中,氧化剂是________,1 mol氧化剂在反应中________(填“得到”或“失去”)________mol电子。
④如果在反应后的溶液中加入NaBiO3,溶液又变紫红色。说出NaBiO3的一个性质:___________________________________________________________________。
(2)某反应体系中的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。
①将氧化剂与还原剂填入下列空格中,并标出电子转移的方向和数目。
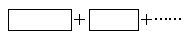
反应中,被还原的元素是________,氧化产物是______________。
②纺织工业中常用氯气作漂白剂,Na2S2O3可作为漂白布匹的“脱氯剂”,Na2S2O3和Cl2反应的产物是H2SO4、NaCl和HCl,则还原剂与氧化剂的物质的量之比为________。
(3)一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗3.2 g CH3OH转移0.6 mol电子,则氧化产物为(填化学式),氧化产物与还原产物的物质的量之比是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com