
【题目】常用于潜水艇或宇宙飞船作供氧剂的是
A. 氧化钠 B. 氯化钠 C. 过氧化钠 D. 碳酸钠
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素质的成分之一,具有香蕉的香味,实验室制备乙酸异戊酯的反应装置示意图和有关数据如下: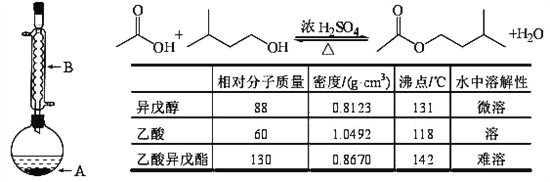
实验步骤:
①在A中加入 4.4 g的异戊醇, 6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A 50分钟,②反应液冷至室温后,倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,③分出的产物加入少量无水硫酸镁固体,静置片刻,过滤除去硫酸镁固体,④进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯 3.77 g。回答下列问题:
(1)异戊醇的系统命名法名称是:________________,
(2)装置B的作用:_____________,
(3)在步骤①中加入过量乙酸的目的是:_____________,
(4)在步骤②洗涤操作中,第一次水洗可以大量洗去的杂质有:___________,
(5)在洗涤、分液操作中,应充分振荡,然后静置,待分层后,先将______从分液漏斗的下口放出,再将______从上口放出,
(6)在步骤③中加入少量无水硫酸镁的目的是:_______________,
(7)本实验的产率是:______,
(8)在步骤④中,若从 130℃开始收集馏分,产率将偏_______(填高或者低)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分金属和非金属材料发现和使用的时间简轴。请回答:
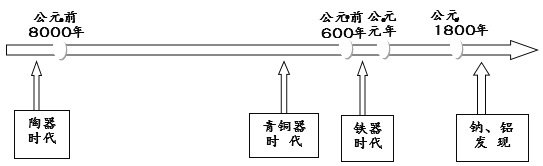
(1)我国最早使用的合金是_________;
(2)Cu、Fe、Na、Al四种金属元素中,金属性最强的是_______(填元素符号);
Al的原子结构示意图是________________________;
(3)我国西汉时期就开始冶炼铜,古人有“曾青得铁则化为铜”的记载,是现代“湿法炼铜”的先驱,请写出上述反应的化学方程式:____________________________;
(4)19世纪初,钠和铝的发现得益于电解技术的应用。
冶炼铝的原料Al2O3属于_____氧化物(选填“酸性”、“碱性”或“两性”);冶炼铝的反应为:2 Al2O3(熔融)![]() 4Al +3O2↑ ,反应中生成1molAl转移电子_________mol。
4Al +3O2↑ ,反应中生成1molAl转移电子_________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子在溶液中能大量共存的是
A. H+、NO3-、CO32- B. K+、Na+、SO42-
C. NH4+、OH-、SO42- D. Ag+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是
A. c(NH4+)=c(SO42﹣)
B. c(NH4+)>c(SO42﹣)
C. c(NH4+)<c(SO42﹣)
D. c(OH﹣)+c(SO42﹣)=c(H+)+c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的5L的密闭固定容积容器中,通入10molNH3,发生了如下反应:N2+3H2![]() 2NH3,反应进行到2min时达到平衡状态,测得容器内有2molN2,求:
2NH3,反应进行到2min时达到平衡状态,测得容器内有2molN2,求:
(1)2min内的平均速率υ(NH3)?
(2)反应前后容器中气体压强之比?
(3)NH3的分解率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A由C、H、O三种元素组成,相对分子质量为90。将9.0 g A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g。A能与NaHCO3溶液发生反应,且2分子A之间脱水可生成六元环化合物。有关A的说法正确的是 ( )
A. 分子式是C3H8O3 B. A催化氧化的产物能发生银镜反应
C. 0.1 mol A与足量Na反应产生2.24 L H2(标准状况) D. A在一定条件下发生缩聚反应的产物是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:2CH3COCH3(l)![]() CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数(反应物已转化为产物的物质的量和反应物总物质的量的比)随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是
CH3COCH2COH(CH3)2(l)。取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数(反应物已转化为产物的物质的量和反应物总物质的量的比)随时间变化的关系曲线(Y-t)如下图所示。下列说法正确的是

A. b代表0℃下CH3COCH3的Y-t曲线
B. 反应进行到20min末,CH3COCH3的v (0℃)/v(20℃)的比值大于1
C. 升高温度可以缩短反应达到平衡的时间并能提高反应物转化为生成物的物质的量
D. 从Y=0到Y=0.113,CH3COCH2COH(CH3)2的Δn(0℃)/Δn(20℃)的比值等于1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【上海市闵行区2017届高三上学期期末教学质量调研(一模)】
利用海水可以提取氯化钠、溴、碘等产品。海带提碘的流程如下:
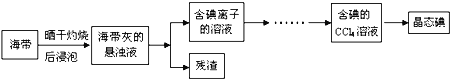
(1)CCl4含有___________键的______________分子(均选填“极性”或“非极性”)。
(2)灼烧海带时除需要三脚架、酒精灯、泥三角外,还需要的主要仪器是____________。
(3)为更好的完成实验,灼烧海带时,需加入一定量的氢氧化钠充分混合后再灼烧。此操作目的是___________________________________。
(4)向盛有碘离子溶液中加入CCl4和氯水,______(填:“上”或“下”)层呈紫红色;如果氯水加过量,CCl4层会由紫红色变成无色。整个过程中被氧化的微粒是__________________。写出并配平CCl4层由紫红色变成无色的化学反应方程式:__________
![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com