
【题目】①分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:

(1)以下叙述中,正确的是__________。
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
(2)变化过程中能量转化的形式主要是:甲为__________;乙为__________。
(3)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式:
_____________________________________________________________
②(4分)氢氧燃料电池,是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)氢氧燃料电池,
(1)如果是碱性燃料电池则负极反应方程式是: .
(2)如果是酸性燃料电池则负极反应方程式是: .
【答案】①(1)C、D(2)化学能转化为热能 化学能转化为电能
(3) Cu2++2e-===Cu②(1) H2+2e﹣+2OH﹣=2H2O (2) H2+2e﹣=2H+
【解析】
试题分析:①(1)A.没有形成闭合回路,不能形成原电池,故A错误;B.铜为金属活动性顺序表H元素之后的金属,不能与稀硫酸反应,甲烧杯中铜片表面没有气泡产生,故B错误;C.两烧杯中硫酸都参加反应,氢离子浓度减小,溶液的pH均增大,故C正确;D.乙能形成原电池反应,较一般化学反应速率更大,所以产生气泡的速率甲中比乙中慢,故D正确;E.原电池电子由负极经外电路流向正极,乙形成原电池,Zn为负极,Cu为正极,则电流方向Cu→Zn,故E错误.故答案为:C、D;(2)甲没有形成闭合回路,不能形成原电池,反应放热,将化学能转变为热能,乙形成闭合回路,形成原电池,将化学能转变为电能;故答案为:化学能转化为热能;化学能转化为电能。(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,是由于锌片不纯,在锌片上形成原电池导致,故答案为:锌片不纯,在锌片上形成原电池;(4)在乙实验中,如果把硫酸换成硫酸铜溶液,Cu2+在正极上得电子被还原产生Cu,电极反应式为Cu2++2e-=Cu,故答案为:Cu2++2e-=Cu;②(1)碱性燃料电池则负极反应方程式为H2+2e-+2OH-=2H2O,故答案为:H2+2e-+2OH-=2H2O;(2)酸性燃料电池则负极反应方程式H2+2e-=2H+;故答案为:H2+2e-=2H+;


科目:高中化学 来源: 题型:
【题目】Ba(NO3)2可用于生产绿色烟花、绿色信号弹、炸药、陶瓷釉药等。钡盐行业生产中排出大量的钡泥[主要含有BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2晶体(不含结晶水),其部分工艺流程如下:
又已知:①Fe3+和Fe2+以氢氧化物形式沉淀完全时,溶液的pH分别为3.2和9.7;
②Ba(NO3)2晶体的分解温度:592℃;
③KSP(BaSO4)=1.1×10-10,KSP(BaCO3)=5.1×10-9。

(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。试用离子方程式说明提纯原理:
。
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,反应的化学方程式为: 。
(3)该厂结合本厂实际,选用的X为 (填序号);
A.BaCl2 B.BaCO3 C.Ba(NO3)2 D.Ba(OH)2
(4)中和I使溶液的p H为4~5目的是 ;结合离子方程式简述原理 。
(5)从Ba(NO3)2溶液中获得其晶体的操作方法是 。
(6)测定所得Ba(NO3)2晶体的纯度:准确称取W克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量其质量为m克,则该晶体的纯度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种元素,已知A元素原子的第一层和第三层电子数相同;B元素原子的第二层比第一层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的原子核外有4个电子层, 第一层与第二层电子数之和等于第三层与第四层电子数之和。写出:
(1)元素符号:A ,B ,C ,D 。
(2)A、D的原子结构示意图 、 ,C的离子结构示意图
化合物AB2的电子式____________ 化学键类型为__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、白藜芦醇的结构简式如下图。它广泛存在于食物(如桑椹、花生,尤其是葡萄)中,可能具有抗癌性。下列有关白藜芦醇的说法正确的是
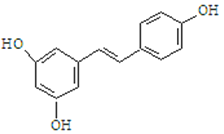
A.该有机物属于醇类
B.1mol该有机物与H2加成时最多消耗1mol H2
C.1mol该有机物与Br2反应时最多消耗6mol Br2
D.1mol该有机物最多消耗3mol NaOH
Ⅱ、根据下列的有机物合成路线回答问题:

(1)写出A、B的结构简式:A 、B 。
(2)写出各步反应类型:
① 、② 、③ 。
(3)写出②、③的反应方程式:
②
③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修2:化学生活与技术]
分析下列水处理方法,完成下列问题:
(1)处理含Cr2O72-工业废水的工艺:
①工艺一:含Cr2O72-的工业废水![]() Cr3+、SO42-
Cr3+、SO42-![]() 。
。
为了进一步除去上述流程中生成的Cr3+,请你设计一个处理方案:________________。
②工艺二:向废水中加入过量的FeSO4溶液,经过一系列反应后,FeSO4溶液和Cr2O72-可形成铁氧体沉淀,从而除去铬元素。若使含1mol Cr2O72-的废水中的Cr2O72-完全转化为一种化学式为Cr0.5Fe2.5O4的铁氧体(其中的铬元素为+3价),理论上需要绿矾(FeSO4·7H2O)的质量不少于
g,上述得到的铁氧体中,Fe3+和Fe2+的个数之比 。
(2)如下是处理含氰(主要以CN—形式存在)废水工艺流程的一部分:
含氰废水![]() 。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为-1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为__________kg(结果保留两位有效数字)。
。发生上述转化后CN—中碳元素转化为+4价,氮元素转化为0价,氯元素转化为-1价,若废水中CN—的浓度为300mg/L,含氰废水的流量为0.8m3/h,为保证安全,实际投放的ClO2为理论值得1.3倍,则为了完成上述过程每小时实际应该投入的ClO2的质量为__________kg(结果保留两位有效数字)。
(3)监测水中氯化物含量可采用硝酸汞滴定法,酸化的水样用硝酸汞滴定时可生成难电离的氯化汞,滴定到终点时过量的汞离子可与指示剂作用使溶液显示紫色。饮用水中的其他物质在通常浓度下对滴定不产生干扰,但水的色质、高价铁、六价铬、硫化物(如S2-)对实验有干扰。
①滴定前常用氢氧化铝悬浊液处理水样,其目的是__________________。
②若水中含有Cr2O72—,常在滴定前向水样中加入一定量的对苯二酚,其目的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种烃,其球棍模型如下图:

(1)等质量的以上物质完全燃烧时耗去O2的量最多的是________(填对应字母,下同);
(2)同状况、同体积的以上三种物质完全燃烧时耗去O2的量最多的是____________;
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是________,生成水最多的是________。
(4)在120℃、1.01×105 Pa下时,有两种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这两种气体是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上用废铁为主要原料生产氧化铁黄的一种工艺流程如下:

(1)氧化铁黄中铁元素的化合价为 ,废铁在反应前常用热的纯碱溶液清洗表面油污,其原理是 (写离子方程式)。
(2)氧化过程生成氧化铁黄的化学方程式是 。
(3)上述流程中,检验“洗涤”是否完全的方法是 。
(4)氧化时应控制pH的合理范围是3.5-4.0,pH过小导致氧化铁黄产率较低的可能原因是 。
(5)取1g样品进行纯度测试,将其溶解于足量稀盐酸中,后用一定浓度的过量NaOH溶液沉淀其中的铁元素,得到沉淀的质量为Bg,试用所给数据求出产品的纯度 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A→F有如下转化关系:

已知:①
②核磁共振氢谱显示C的分子中含有4种不同化学环境的氢原子,且峰面积之比为3:2:2:1。
③F是酯类化合物,分子中苯环上的一溴代物只有两种。
(1)A的分子式是 ,主要用途是 (写一种)。
(2)检验B中官能团的常用方法是 。
(3)D物质的名称为 。
(4)C+E→F的化学方程式是 。
(5)X与E互为同分异构体,且X有下列性质,符合条件的X有 种。
①接触NaHCO3有二氧化碳气体产生。
②与银氨溶液共热有银镜现象。
③1摩尔X与足量钠反应有1摩尔气体产生。
(6)Y与E也互为同分异构体,属于酯类化合物,分子中只含一种官能团,且苯环上的一硝基取代物只有一种,则Y的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,其中的编号代表所对应的元素。请回答下列问题:

(1)⑧号元素的基态原子的价电子排布式是_________________,与其同周期,且基态原子的核外未成对电子数最多的元素是_______________(写出元素符号)。
(2)④号与⑦号元素形成的氧化物的熔点由高到低的是_________________。
(3)①号与③号元素形成的含有18电子的分子为___________(写出名称),该分子中③元素的原子的杂化方式为______________。②、④、⑧三种元素的原子形成的晶体,其晶胞的结构特点如图所示,则该化合物的化学式为______________(用对应的元素符号表示)。

(4)下表是某些短周期元素的电负性值:
元素符号 | Li | Be | B | C | O | F | Na | Al | Si | P | S | Cl |
X值 | 1.0 | 1.5 | 2.0 | 2.5 | 3.5 | 4.0 | 0.9 | 1.5 | 1.8 | 2.58 | 2.5 | 3.1 |
①通过分析电负性值变化规律,确定N最接近的电负性值范围:________<N<__________
②推测电负性值与原子半径关系是____________________;
③试判断:AlBr3中化学键类型是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com