
分析 A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大.已知A和B原子有相同的电子层数,则A、B处于同一周期,且A的L层电子数是K层电子数的两倍,则A有2个电子层,L层电子数为4,故A为碳元素;C单质燃烧时呈现黄色火焰,则C为钠元素;C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,则B为氧元素,D为硫元素,据此解答.
解答 解:A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大.已知A和B原子有相同的电子层数,则A、B处于同一周期,且A的L层电子数是K层电子数的两倍,则A有2个电子层,L层电子数为4,故A为碳元素;C单质燃烧时呈现黄色火焰,则C为钠元素;C的单质在点燃时与足量的B单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,则B为氧元素,D为硫元素.
(1)通过以上分析知,A是C,B是O,C是Na,D是S,
故答案为:C;O;Na;S;
(2)钠与氧气在高温下反应生成过氧化钠,反应方程式为:2Na+O2$\frac{\underline{\;高温\;}}{\;}$Na2O2,
故答案为:2Na+O2$\frac{\underline{\;高温\;}}{\;}$Na2O2;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>S>O,
故答案为:Na>S>O;
(4)SO2由不同的非金属元素形成,属于属于共价化合物,
故答案为:共价.
点评 本题考查结构性质位置关系应用,关键是根据核外电子排布、元素化合物性质推断元素,比较基础.


科目:高中化学 来源: 题型:选择题
| A. | 含非极性键的分子一定是非极性分子 | |
| B. | 含有极性键的分子一定是极性分子 | |
| C. | 非极性分子一定含有非极性键 | |
| D. | 极性分子不一定只含有极性键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
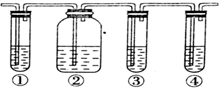
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性高锰酸钾溶液鉴别直馏汽油与裂化汽油 | |
| B. | 用溴水鉴别苯、甲苯 | |
| C. | 用燃烧方法鉴别聚乙烯、聚氯乙烯 | |
| D. | 用溴水鉴别苯、硝基苯和苯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
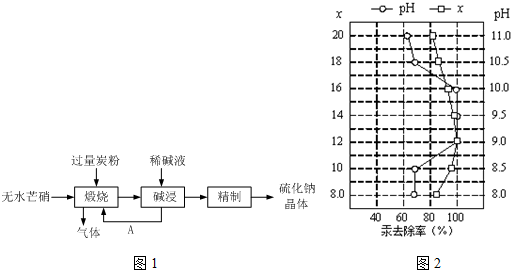
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4和C6H6 | B. | CH4 和C3H8 | C. | C6H6和CH4 | D. | CH4和CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
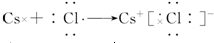 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com