
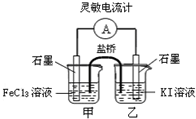
| A. | 反应开始时,乙中电极反应为2I-+2e-═I2 | |
| B. | 反应开始时,甲中石墨电极上发生氧化反应 | |
| C. | 电流表指针为零时,两池溶液颜色相同 | |
| D. | 平衡时甲中溶入FeCl2固体后,乙池的石墨电极为正极 |
分析 根据常温下能自动发生的氧化还原反应都可设计成原电池,再利用总反应2Fe3++2I-?2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的石墨作正极,乙烧杯中的石墨作负极,利用负极发生氧化反应,正极发生还原反应,并利用平衡移动来分析解答.
解答 解:A、因乙中I-失去电子放电,元素的化合价升高,发生氧化反应,乙中石墨电极上发生的电极反应式为:2I--2e-═I2,故A错误;
B、由总反应方程式知,Fe3+被还原成Fe2+,则甲中Fe3+发生还原反应,故B错误;
C、当电流计为零时,乙中生成单质碘,溶液呈黄色,甲中含有Fe3+呈黄色,所以两池溶液颜色相同,故C正确;
D、当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故D正确;
故选CD.
点评 本题是对原电池原理综合考查,并注重与化学平衡的联系,学生明确原电池的工作原理、正负极的判断方法、化学平衡的移动即可解答.


 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:多选题
| A. |  制取Cl2用 制取Cl2用 | |
| B. |  可完成“喷泉”实验 可完成“喷泉”实验 | |
| C. |  制取干燥的NH3 制取干燥的NH3 | |
| D. |  分离石油,得到汽油、煤油和柴油等各种馏分 分离石油,得到汽油、煤油和柴油等各种馏分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为比较Cl与S元素的非金属性强弱,相同条件下,测定相同浓度的NaCl溶液和Na2S溶液的pH值 | |
| B. | 为观察Mg条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部 | |
| C. | 为验证盐桥的作用,在两个烧杯中分别盛适量硫酸亚铁铵和稀酸性高锰酸钾溶液,分别插入石墨棒用导线与电流计相连,然后用装有K2SO4饱和溶液的琼脂的U型管两端插入两个烧杯中,电流计偏转,一段时间后高锰酸钾溶液褪色 | |
| D. | 为测定一定浓度的NaOH溶液放置空气中是否部分转化为Na2CO3,用甲基橙作指示剂用标准盐酸溶液滴定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁粉加到稀硝酸中 | |
| B. | 向稀盐酸中滴入少量的NaAlO2溶液 | |
| C. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| D. | NaOH溶液与醋酸溶液反应后所得的pH大于7的溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后溶液中Fe3+物质的量为0.6mol | |
| B. | 反应后产生13.44L H2(标准状况) | |
| C. | 反应后溶液中Fe2+和Fe3+物质的量之和为0.8mol | |
| D. | 由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com