
| A. | 硫化钠溶液显碱性:S2-+H2O═HS-+OH- | |
| B. | 硫酸铜溶液呈酸性:Cu2++2H2O?Cu(OH)2↓+2H+ | |
| C. | 氯化铝溶液与碳酸钠溶液混合:Al3++CO32-═Al(OH)3↓+H2↑ | |
| D. | 在饱和氯化铵溶液中撒入镁粉后微热:2NH4++Mg═Mg2++2NH3↑+H2↑ |
分析 A.硫离子水解分步进行,以第一步为主,为可逆反应;
B.铜离子水解显酸性,为可逆反应,但不生成沉淀;
C.发生相互促进水解反应生成沉淀和二氧化碳气体;
D.Mg与氯化铵反应生成氯化镁、氨气、氢气.
解答 解:A.硫化钠溶液显碱性的离子反应为S2-+H2O?HS-+OH-,故A错误;
B.硫酸铜溶液呈酸性的离子反应为Cu2++2H2O?Cu(OH)2+2H+,故B错误;
C.氯化铝溶液与碳酸钠溶液混合的离子反应为3H2O+2Al3++3CO32-═2Al(OH)3↓+3CO2↑,故C错误;
D.在饱和氯化铵溶液中撒入镁粉后微热的离子反应为2NH4++Mg═Mg2++2NH3↑+H2↑,故D正确;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意水解离子反应的特点,题目难度不大.


科目:高中化学 来源: 题型:填空题
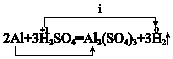 有四种物质:①氧化铝 ②稀硫酸 ③碳酸氢钠 ④氢氧化钠
有四种物质:①氧化铝 ②稀硫酸 ③碳酸氢钠 ④氢氧化钠查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
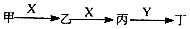 甲、乙、丙、丁四种物质中,丁为难溶于水的物质,在一定条件下,它们之间具有如图转化关系(部分反应物、生成物和反应条件未列出).下列有关物质的推断不正确的是( )
甲、乙、丙、丁四种物质中,丁为难溶于水的物质,在一定条件下,它们之间具有如图转化关系(部分反应物、生成物和反应条件未列出).下列有关物质的推断不正确的是( )| A. | 若甲为C,则Y可能是Ba(OH)2溶液 | B. | 若甲为CO2,则Y可能是FeCl3溶液 | ||
| C. | 若甲为NH3,则Y可能是NaOH | D. | 若甲为S,则Y可能是BaC12溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2SO4(浓)+C | B. | Fe3O4+Al | C. | Cl2+Mg | D. | NO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 干冰中分子的堆积方式为非密堆积 | |
| B. | 金属晶体中原子的最大配位数为12 | |
| C. | 晶体硅熔化时需破坏非极性共价键 | |
| D. | 冰融化为水的过程中其密度先变大,超过4℃后又逐渐变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 坩埚质量 | 坩埚+试样 | 失水后,坩埚+试样 |
| 11.70g | 20.82g | 16.50g |
| A. | 晶体中含不挥发杂质 | B. | 未做恒重操作 | ||
| C. | 加热前晶体未研磨 | D. | 加热时有晶体溅出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com