
| A、家庭用的“84”消毒液与洁厕灵不能同时混合使用,否则会发生中毒事故 |
| B、在牙膏中添入Na2PO3F、NaF能防治龋齿,当提供的氟离子浓度相等时,它们防治龋齿的作用是相同的 |
| C、侯氏制碱法的工艺过程中主要应用了物质熔沸点的差异 |
| D、可用蘸浓盐酸的玻璃棒检验输送氨气的管道是否漏气 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 装置:除去二氧化碳中的少量氯化氢气体 装置:除去二氧化碳中的少量氯化氢气体 |
B、 装置:加热乙醇、乙酸和浓硫酸的混合液制取乙酸乙酯 装置:加热乙醇、乙酸和浓硫酸的混合液制取乙酸乙酯 |
C、 装置:用酸性高锰酸钾溶液滴定过氧化氢溶液 装置:用酸性高锰酸钾溶液滴定过氧化氢溶液 |
D、 装置:用水吸收氯化氢气体 装置:用水吸收氯化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
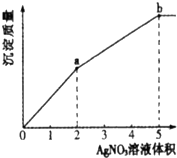 往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法正确的是( )
往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示.下列说法正确的是( )| A、KSP(AgCl)<KSP(AgI) |
| B、c( Cl-):c( I-)=3:2 |
| C、m( AgCl ):m( AgI )=2:3 |
| D、a~b段产生黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Br- |
| B、SO42- |
| C、HSO3- |
| D、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯和甲烷都能发生加成反应 |
| B、CuSO4溶液能使鸡蛋清盐析而沉淀 |
| C、米酒变酸是因为乙醇被氧化为乙酸 |
| D、HNO3不能与苯发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 理由 | 结论 |
| A | 共价键强弱:O-H>S-H | 沸点:H2O>H2S |
| B | 元素的非金属性:Cl>S | 酸性:HCl>H2S |
| C | 相同外界条件下反应速率:a反应>b反应 | 活化能:b反应>a反应 |
| D | 还原性:Fe>Cu | 氧化性:Fe3+>Cu2- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com