
分析 由信息可知,该物质能分解,水解显碱性,与酸反应生成二氧化碳,则甲中物质为碳酸氢钠,
(1)推测该胃药含有的主要化学成份是NaHCO3,焙制糕点用的发酵粉;
(2)碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳;
(3)根据镁元素、硅元素、和氢元素的化合价以及氧化物的定义进行书写.
解答 解:(1)由信息可知,该物质能分解,水解显碱性,与酸反应生成二氧化碳,则甲中主要物质为碳酸氢钠,其化学式为NaHCO3,焙制糕点用的发酵粉,故答案为:NaHCO3;焙制糕点用的发酵粉;
(2)碳酸氢钠与盐酸反应生成氯化钠、水、二氧化碳,该反应的离子方程式为HCO3-+H+═CO2↑+H2O,
故答案为:HCO3-+H+═CO2↑+H2O;(2)HCO3-+H+=H2O+CO2↑
(3)镁元素显+2价,硅元素显+4价,氢元素显+1价,氧元素显-2价,氧化物中只有氧和另一种元素,故答案为:2MgO•3SiO2•nH2O.
点评 在解此类题时,首先读懂题意,然后结合学过的知识和题中的知识进行解答,需要注意物质的量的求解.


科目:高中化学 来源: 题型:解答题
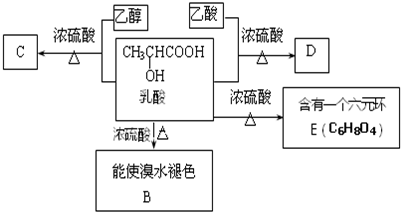
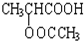 ;
;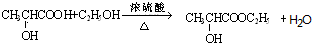 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu→CuCl2 | B. | CuO→Cu2O | C. | Cu(OH)2→CuO | D. | CuO→Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CO2 | B. | COCl2 | C. | C2H6O | D. | H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡前,随着反应的进行,容器内压强变小 | |
| B. | 平衡时,其他条件不变,分离出H2O(g),逆反应速率减小 | |
| C. | 平衡时,其他条件不变,升高温度平衡常数增大 | |
| D. | 其他条件不变,使用不同催化剂,HCl(g)的转化率不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com