
| A. | 用食醋除去暖瓶内的水垢 | |
| B. | 鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀 | |
| C. | 淀粉溶液中加碘水变蓝 | |
| D. | 棉花织品和羊毛织品:分别灼烧闻气味 |
分析 A.用食醋除去暖瓶内的水垢是醋酸与氢氧化镁、碳酸钙反应生成可溶性盐的过程;
B.鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀,该过程属于蛋白质的盐析;
C.淀粉遇碘单质变蓝,该过程淀粉遇碘反应生成络合物;
D.燃烧有新物质生成.
解答 解:A.用食醋除去暖瓶内的水垢是醋酸与氢氧化镁、碳酸钙反应生成可溶性盐的过程,有新物质生成属于化学变化,故A错误;
B.鸡蛋白溶液中加入硫酸铵饱和溶液后析出白色沉淀,该过程属于蛋白质的盐析,没有新物质的产生,属于物理过程,故B正确;
C.淀粉遇碘单质变蓝,该过程淀粉遇碘反应生成络合物,有新的物质生成,属于化学变化,故C错误;
D.燃烧有新物质生成,属于化学变化,故D错误.
故选B.
点评 本题考查了物理变化与化学变化的判断,题目难度不大,抓住是否有新的物质生成是解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 22.4 L 乙烯和丙烯的混合气体中分子数为NA | |
| B. | 一定温度下,15 g甲醛和葡萄糖的混合物含O原子数为0.5 NA | |
| C. | 常温常压下,8.8 g乙酸乙酯中含有C-O键的个数为0.5 NA | |
| D. | 4 mL 15 mol•L-1浓硝酸与足量铜反应,生成NO2的分子数约为0.03 NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 H4SiO4 | B. | Cl2O HClO4 | C. | Mn2O7 HMnO4 | D. | N2O5 HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:在卡片上,描述合理的是( )| A. | ①②③ | B. | ③④⑤ | C. | ④⑤⑥ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 臭氧、乙醇溶液均可用于消毒杀菌且原理完全相同 | |
| B. | 半导体材料和光纤制品都是以硅为基本原料生产的 | |
| C. | 煤的干馏和石油的分馏均属化学变化 | |
| D. | 亚硝酸盐、二氧化硫均可以用作食品的防腐剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
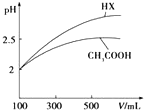 已知25℃时部分弱电解质的电离平衡常数数据如表所示:
已知25℃时部分弱电解质的电离平衡常数数据如表所示:| 化学式 | CH3COOH | H2CO3 | HClO | |
| 电离平衡常数 | Ka=1.8×10-5 | Kal=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com