
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
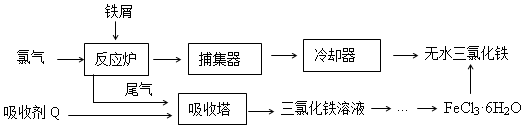
分析 氯气与铁在反应炉中反应生成氯化铁,尾气用吸收剂Q处理得到氯化铁,故Q为氯化亚铁,氯化铁溶液蒸发浓缩、冷却结晶得到氯化铁晶体,为防止氯化铁水解,在HCl气流中加热蒸干氯化铁晶体得到氯化铁,
(1)因为铁离子易水解所以应在通HCl气体的氛围下加热;
(2)由表中数据可知,温度越高氯化铁的溶解度越高,由溶液获得晶体需加热浓缩、冷却结晶、过滤、洗涤、干燥;
(3)依据沉淀溶解平衡的溶度积,结合溶液PH计算得到;
(4)①KI溶液与FeCl3发生氧化还原反应生成碘单质和二价铁;
②12.50mLNa2S2O3溶液含有Na2S2O3物质的量为12.50×10-3 L×0.1000mol•L-1=1.25×10-3mol,根据关系式2Fe3+~I2~S2O32-计算n(Fe3+),氯化铁的物质的量等于n(Fe3+),利用m=nM计算氯化铁的质量,根据质量分数定义计算.
解答 解:(1)因为Fe3+易水解生成挥发性的HCl,所以由FeCl3•6H2O晶体得到无水FeCl3,应在氯化氢气流中加热FeCl3•6H2O晶体,得到无水FeCl3,
故答案为:在通HCl气体的氛围下加热;
(2)由表中数据可知,温度越高氯化铁的溶解度越高,由溶液获得晶体需加加热浓缩,再冷却结晶;故答案为:加热浓缩;冷却结晶;
(3)当溶液pH为4时,溶液中c(OH-)=10-10mol/L,Ksp[Fe(OH)3]=c(Fe3+)•c3(OH-)=2.6×10-39,所以溶液中c(Fe3+)=$\frac{2.6×10{\;}^{39}}{(10{\;}^{-10}){\;}^{3}}$=2.6×10-9 mol•L-1,故答案为:2.6×10-9;
(4)①KI溶液与FeCl3发生氧化还原反应生成碘单质和二价铁,离子方程式为:2Fe3++2I-=2Fe2++I2;故答案为:2Fe3++2I-=2Fe2++I2;
②12.50mLNa2S2O3溶液含有Na2S2O3物质的量为12.50×10-3 L×0.1000mol•L-1=1.25×10-3mol,则:
根据关系式:2Fe3+~~~~~I2~~~~~~2S2O32-
2 2
n(Fe3+) 1.25×10-3mol×10
所以 n(Fe3+)=1.25×10-3mol×10=1.25×10-2mol,
所以2.300g无水氯化铁样品中氯化铁的质量为1.25×10-2mol×162.5g/mol=2.03125g
所以2.300g无水氯化铁样品中氯化铁的质量分数为$\frac{2.03125g}{2.300g}$×100%=88.32%;
故答案为:88.32%.
点评 本题考查学生对工艺流程的理解、物质的分离提纯等基本操作、氧化还原反应滴定应用、溶度积有关计算等,难度中等,需要学生具有扎实的基础知识与灵活运用知识解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Mg2+、SO42-、NO3- | B. | K+、Mg2+、SO42+、Cl- | ||
| C. | Ag+、Na+、NO3-、Cl- | D. | NH4+、Ba2+、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
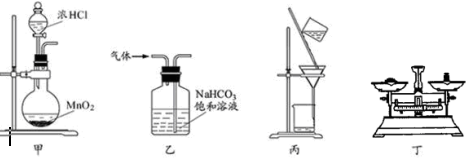
| A. | 用装置甲制取氯气 | |
| B. | 用装置乙除去氯气中的少量氯化氢 | |
| C. | 用装置丙分离出MnCl2溶液中的固体MnO2 | |
| D. | 用装置丁称得回收的二氯化锰质量为5.36g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 乙、丙都能发生银镜反应 | |
| B. | 用FeCl3溶液鉴别甲、丙两种有机化合物 | |
| C. | 甲分子中所有碳原子可能共平面 | |
| D. | 甲、乙、丙三种有机化合物均可与NaOH溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 23:12:9 | C. | 9:12:23 | D. | 36:69:92 |
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:推断题
某芳香烃A,分子式为C8H10,B、C的混合物在NaOH乙醇溶液中加热可以生成同一种有机物Y,以Y为单体可以合成高分子化合物。某烃类衍生物X,分子式为C15H14O3,遇FeCl3溶液显紫色;J分子内有两个互为对位的取代基。在一定条件下有如下的转化关系(无机物略去):

(1)一种属于芳香烃类的A的同分异构体,其苯环上的一氯代物仅有一种,其结构简式为 。
(2)J中所含的含氧官能团的名称为__________________。
(3)E与H反应的化学方程式是_______________,反应类型是_____________。
(4)已知J有多种同分异构体,写出一种符合下列性质的J的同分异构体的结构简式:_________________________。
① 与FeCl3溶液作用显紫色
② ②与新制Cu(OH)2悬浊液作用产生红色沉淀
③ ③苯环上的一卤代物有2种
查看答案和解析>>
科目:高中化学 来源:2017届吉林省高三上第二次模拟化学试卷(解析版) 题型:选择题
根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、 干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是

查看答案和解析>>
科目:高中化学 来源:2016-2017学年云南省高一9月月考化学卷(解析版) 题型:选择题
在Cu+4HNO3(浓)= Cu(NO3)2+2NO2↑+2H2O,下列有关该反应说法正确的是
A.硝酸表现出了氧化性和酸性 B.还原剂与氧化剂之比为1:4
C.每个硝酸分子得到2个电子 D.硝酸铜是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com