
下列离子反应方程式书写正确的是( )
A.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.向NaAlO2溶液中通入过量二氧化碳:AlO2-+CO2+2H2O=Al(OH)3+HCO3-
C.在强碱溶液中次氯酸钠与氢氧化铁反应生成Na2FeO4:
3ClO2-+2Fe(OH)3=2FeO42-+3Cl-+4H+
D.向硫化钠溶液中滴入氯化铝溶液:2Al3++3S2-=Al2S3↓
科目:高中化学 来源:2016届浙江省嘉兴、杭州、宁波五校高三上第一次联考化学试卷(解析版) 题型:选择题
利用下图M、N两个装置进行相关实验,下列有关说法正确的是
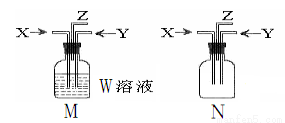
选项 | 所用装置 | 描述 | 结论 |
A | M | W:BaCl2 ;X:CO2 Y:SO2 | M中有白色沉淀生成 |
B | M | W:饱和食盐水;先通入X:CO2,再通入Y:NH3 | M中制得小苏打 |
C | N | X:NH3 Y:Cl2 | Z出口有白烟产生 |
D | N | X:NH3 Y:O2 | Z出口有红棕色气体 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
下列关于煤、石油、天然气等资源的说法正确的是( )
A.石油裂解得到的汽油是纯净物
B.石油产品都可用于聚合反应
C.天然气是一种清洁的化石燃料
D.水煤气是通过煤的液化得到的气体燃料
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
氨基钠和氢化钠与水反应的化学方程式如下:①NaNH2+H2O=NaOH+NH3↑
②NaH+H2O==NaOH+H2↑,下列叙述正确的是
A.氨基钠和氢化钠与盐酸反应都只生成一种盐
B.方程式②中,每生成1mol H2转移1 mol电子
C.氨基钠和氢化钠的晶体中都只含离子键
D.方程式①中,氨基钠是还原剂
查看答案和解析>>
科目:高中化学 来源:2016届云南师大附中高考适应性月考(四)理综化学试卷(解析版) 题型:选择题
分子式为C6H12O2,属于酯类,且能发生银镜反应的同分异构体有
A.8种 B.9种 C.10种 D.11种
查看答案和解析>>
科目:高中化学 来源:2016届山西平遥中学等重点中学高三第三次练兵化学试卷(解析版) 题型:选择题
稀土金属铈(Ce)在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:①铈常见的化合价为+3和+4价;②氧化性:Ce4+> Ce3+。下列说法正确的是
A.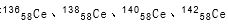 它们互称同素异形体
它们互称同素异形体
B.铈溶于氢碘酸的主要化学方程式可表示为2Ce+6HI=2CeI3+3H2↑
C.工业上可以采用电解氯化铈水溶液来获得铈单质
D.工业上金属铈一般保持在敞口容器中
查看答案和解析>>
科目:高中化学 来源:2016届宁夏回族自治区银川一中高三上第五次月考理化学试卷(解析版) 题型:填空题
硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图1。
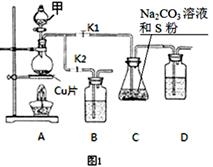
已知:Na2S2O3在酸性溶液中不能稳定存在。
(1)步骤1:打开K1、关闭K2,向圆底烧瓶中加入足量甲并加热,写出反应的方程式: 。
(2)步骤2:始终保持C中溶液呈碱性,反应一段时间后,硫粉的量逐渐减少,打开K2、关闭K1并停止加热。
①C中溶液须保持呈碱性的原因:若呈酸性,则 、 。(用离子方程式表示)
②装置B、D的试剂相同,均为 。
步骤3:将C中所得混合物分离提纯后得产品。
(3)利用反应2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2也能制备Na2S2O3。所需仪器如图2,按气流方向连接各仪器,接口顺序为:a→____,____→ , → , →d。
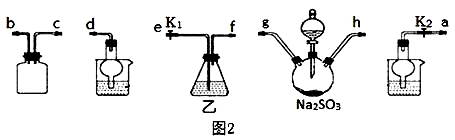
(4)装置乙盛装的试剂是:_____________________________。
(5)Na2S2O3还原性较强,工业上常用作除去溶液中残留的Cl2,该反应的离子方程式为 。
(6)请设计简单的实验方案,证明上述残留的Cl2被还原成了Cl—:____________
查看答案和解析>>
科目:高中化学 来源:2016届河北正定中学高三上学期第五次月考理科综合化学试卷(解析版) 题型:选择题
下列对定量实验误差分析正确的是
A.中和热测定实验中,缓慢地将NaOH溶液倒入测定装置中——测定结果无影响
B.酸碱中和滴定实验中,滴定前无气泡而滴定后有气泡——测定结果偏高
C.测定溶液pH的实验中,用干燥pH试纸测定新制氯水的pH——测定结果无影响
D.现需90 mL 1.0 mol/L NaOH溶液,称取3.6 g NaOH 固体配制——溶液浓度偏低
查看答案和解析>>
科目:高中化学 来源:2015-2016北京大学附中宇华教育集团高二12月化学卷(解析版) 题型:填空题
(1)一定温度下,有a.盐酸;b.硫酸;c.醋酸三种酸,用字母填写下列空格:
①当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是________________________。
②若三者c(H+)相同时,物质的量浓度由大到小的顺序是_________________________。
(2)常温下,0.1 mol·L-1的HCl溶液中,由水电离出来的H+浓度为________mol·L-1。
(3)在一元强碱MOH溶液中加入一元酸HA溶液,充分反应后,溶液呈中性。甲同学认为溶液中c(A-)=c(M+),而乙同学认为c(A-)和c(M+)是否相等,要看一元酸HA是强酸还是弱酸。你认为__________同学的说法正确,理由是____________________________。
(4)明矾[KAl(SO4)2·12H2O]常用作净 水剂,其原理是_______________(用离子方程式表示)。
水剂,其原理是_______________(用离子方程式表示)。
(5)将FeCl3溶液蒸干并灼烧,最终得到的固体物质是______________________(填写化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com