
【题目】硫酸和盐酸组成的混合液100.0 mL,向其中加入氢氧化钡粉末4.275g,充分反应后,经过滤、洗涤、干燥,得到沉淀2.330g,同时测得滤液中的OH-离子浓度为0.100 mol·L-1 。(设溶液总体积始终不变)请列式计算
(1)原溶液中硫酸的物质的量为____________。
(2)原混合液中盐酸的物质的量浓度_______________。
(3)若将原硫酸和盐酸混合溶液100ml与足量金属锌反应,则在标况下产生的气体体积为______________。
【答案】(1)0.01mol (2)0.2mol/L (3)0.448L
【解析】
试题分析:(1)充分反应后,得到硫酸钡沉淀2.330g,因此H2SO4的物质的量为:![]() ,故硫酸的物质的量为0.01mol;(2)加入溶液中的氢氧化钡粉末质量为4.275g,,则物质的量为:
,故硫酸的物质的量为0.01mol;(2)加入溶液中的氢氧化钡粉末质量为4.275g,,则物质的量为:![]() ;测得滤液中的OH-离子浓度为0.100 mol·L-1 ,则OH-离子的物质的量为:0.01mol,故溶液中剩余氢氧化钡的物质的量为0.005mol;由(1)可知,与硫酸反应的氢氧化钡的物质的量为0.01mol,因此与盐酸反应的氢氧化钡的物质的量为0.01mol,原混合液中盐酸的物质的量为:
;测得滤液中的OH-离子浓度为0.100 mol·L-1 ,则OH-离子的物质的量为:0.01mol,故溶液中剩余氢氧化钡的物质的量为0.005mol;由(1)可知,与硫酸反应的氢氧化钡的物质的量为0.01mol,因此与盐酸反应的氢氧化钡的物质的量为0.01mol,原混合液中盐酸的物质的量为:![]() ,盐酸的物质的量浓度为:
,盐酸的物质的量浓度为:![]() ;(3)原混合液中硫酸的物质的量浓度为
;(3)原混合液中硫酸的物质的量浓度为![]() ,因此原硫酸和盐酸混合溶液100ml中氢离子的物质的量为:
,因此原硫酸和盐酸混合溶液100ml中氢离子的物质的量为:![]() ,与足量金属锌反应,根据得失电子守恒,可知,在标准状况下生成氢气的体积为
,与足量金属锌反应,根据得失电子守恒,可知,在标准状况下生成氢气的体积为![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示(己知硝酸只被还原为NO气体)。下列分析或结果错误的是
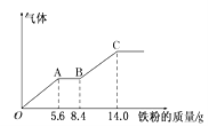
A.H2SO4浓度为2.5mol·L-1
B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气
C.第二份溶液中最终溶质为FeSO4
D.原混合酸中NO3-的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要是由以下什么因素决定的
① 气体分子的直径② 气体物质的量的多少
③ 气体分子间的平均距离④ 气体分子的相对分子质量
A.①② B.①③ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100mL浓度为2mol.L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气的总量,可采用的方法是
A.加入适量6 mol.L-1的盐酸
B.加入少量醋酸钠固体
C.加热
D.加入少量金属钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.1 mol氧含有6.02 ×l023个微粒 B.阿伏加德罗常数数值约等于6.02×l0 23
C.硫的摩尔质量等于它的相对原子质量 D.CO2的摩尔质量为44g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学-物质结构与性质】
配位化合物为深蓝色晶体,由原子序数依次增大的A、B、C、D、E五种元素组成,其原子个数比为l4:4:5:1:1。其中C、D元素同主族且原子序数D为C的二倍,E元素的外围电子排布为(n-1)dn+6nsl,回答下列问题。
(1)写出元素D在周期表中的位置是 ,B原子的外围电子排布图 。E原子的核外有 种不同运动状态的电子,B和C的第一电离能大小关系 。(用元素符号表示)
(2)C元素可与A元素形成两种常见的化合物,其原子个数比分别为1:1和l:2,画出原子个数比为1:1的化合物的电子式 ,两种化合物可任意比互溶,解释其主要原因为 。
(3)该配位化合物的化学式为 。
(4)A元素与B元素可形成分子式为A2B2的某化合物,该化合物的分子具有平面结构,则其结构式为 。
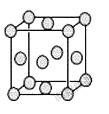
(5)已知E的晶胞结构如图所示,此晶胞立方体的边长为a cm,E单质的密度为pg.cm-3,则阿伏伽德罗常数为 (用a、p表示)。该晶胞配位数为 ,EDC4常作电镀液,其中DC![]() 的空间构型是 ,其中D原子的杂化轨道类型是 。若电解EDC4的水溶液,则电解总反应的化学方程式为 。
的空间构型是 ,其中D原子的杂化轨道类型是 。若电解EDC4的水溶液,则电解总反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是生命之源,下列关于水的说法正确的是
A. 水是弱电解质
B. 可燃冰是可以燃烧的水
C. 氢氧两种元素只能组成水
D. 0℃时冰的密度比液态水的密度大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】经常有人因误食亚硝酸钠(NaNO2)而中毒。原因是NaNO2像食盐一样既有咸味,又有很强毒性。已知亚硝酸钠能发生如下反应:
2NaNO2+4HI=2NO+I2+2NaI+2H2O
(1)该反应的氧化剂是_______,被氧化的是_________元素。
(2)若此反应中电子转移数目为0.5mol,则被氧化的还原剂的物质的量为___________。
(3)用双线桥标出上述反应的电子转移的方向和数目。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验装置进行的相应实验,能达到实验目的的是
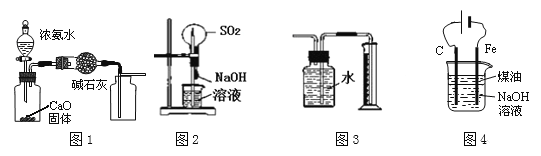
A.用图1装置制取并收集干燥纯净的NH3
B.用图2装置可以完成“喷泉”实验
C.用图3装置直接测量Cu与浓硝酸反应产生的NO2体积
D.用图4装置制备Fe(OH)2并能较长时间观察其颜色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com