
下列离子方程式正确的是( )
A. 苏打溶液与稀盐酸反应的离子反应方程式:HCO3﹣+H+═CO2↑+H2O
B. Fe2O3与HI:Fe2O3+6H+═2Fe3++3H2O
C. NaHCO3溶液中滴加少量澄清石灰水:2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣
D. 浓烧碱溶液中加入铝片:Al+OH﹣+H2O═AlO2﹣+H2↑
考点: 离子方程式的书写.
分析: A.苏打为碳酸钠;
B.发生氧化还原反应生成碘化亚铁、碘和水;
C.石灰水完全反应,生成碳酸钙、碳酸钠和水;
D.电子、原子不守恒.
解答: 解:A.苏打溶液与稀盐酸反应的离子反应方程式为CO32﹣+2H+═CO2↑+H2O,故A错误;
B.Fe2O3与HI的离子反应为Fe2O3+2I﹣+6H+═2Fe2++I2+3H2O,故B错误;
C.NaHCO3溶液中滴加少量澄清石灰水的离子反应为2HCO3﹣+Ca2++2OH﹣═CaCO3↓+2H2O+CO32﹣,故C正确;
D.浓烧碱溶液中加入铝片的离子反应为2Al+2OH﹣+2H2O═2AlO2﹣+3H2↑,故D错误;
故选C.
点评: 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及复分解反应的离子反应考查,注意离子反应中保留化学式的物质,题目难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:
下列与有机结构、性质相关的叙述中,正确的是( )
|
| A. | 油脂水解的产物是氨基酸和甘油 |
|
| B. | 乙烯和聚乙烯均能和溴水发生加成反应而使溴水褪色 |
|
| C. | 乙醇、乙酸、乙酸乙酯可以用饱和碳酸钠溶液鉴别 |
|
| D. | 蛋白质、淀粉、纤维素、蔗糖都属于有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应N2(g)+3H2(g)⇌2NH3(g)在体积不变的密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n mol N2 的同时,生成3n mol H2
②断开1mol H﹣H键的同时断开2molN﹣H键
③用N2、H2、NH3的浓度变化表示的反应速率之比为1:3:2
④混合气体的压强不再改变
⑤混合气体的密度不再改变.
A. ②④ B. ①④ C. ①③④ D. ②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
仔细分析下列表格中烃的排列规律,判断排列在第15位烃的分子式是( )
1 2 3 4 5 6 7 8 9 …
C2H2 C2H4 C2H6 C3H4 C3H6 C3H8 C4H6 C4H8 C4H10
A. C6H12 B. C6H14 C. C7H12 D. C7H14
查看答案和解析>>
科目:高中化学 来源: 题型:
食品香精菠萝酯的生产路线(反应条件略去)如下:

下列叙述错误的是( )
A. 步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B. 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应
C. 苯氧乙酸和菠萝酯均可与NaOH溶液发生反应
D. 步骤(2)产物中残留的丙烯醇可用溴水检验
查看答案和解析>>
科目:高中化学 来源: 题型:
关于 Na2CO3和NaHCO3下列说法不正确的是( )
A. 可以用加热的方法除去Na2CO3中的NaHCO3
B. 分别向Na2CO3和NaHCO3溶液滴加少量盐酸,产生CO2气体较快的为NaHCO3
C. 可以用Ca(OH)2溶液区分Na2CO3和NaHCO3溶液
D. Na2CO3比NaHCO3易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物.
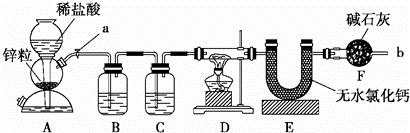
(1)如何检查装置A的气密性?
(2)装置A发生的反应有时要向其中加入少量CuSO4溶液,其目的是
(3)为了安全,在点燃D处的酒精灯之前,在b出口处必须 .
(4)装置B的作用是 ;装置C中装的液体是 .
(5)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双通玻璃管中发生反应的化学方程式是
(6)若FeO和Fe2O3固体混合物的质量为23.2g,反应完全后U型管的质量增加7.2g,则混合物中Fe2O3的质量为 g.
(7)U形管E右边又连接干燥管F的目的是 ,若无干燥管F,测得Fe2O3的质量将 (填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
在一固定体积的密闭容器中,充入2 mol CO2和1 mol H2发生如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数与温度(T)的关系如下表:
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=__________________________________。
(2)若反应在830 ℃下达到平衡,则CO2气体的转化率为________。
(3)若绝热时(容器内外没有热量交换),平衡发生移动的结果是使容器内CO的浓度增大,则容器内气体温度______(填“升高”、“降低”或“不能确定”)。
(4)能判断该反应是否达到化学平衡状态的依据是______。
A.容器内压强不变
B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
E.c(CO2 )·c(H2)=c(CO)·c(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com