
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2011-2012学年安徽省蚌埠市三年级第一次教学质量检查考试化学试卷(解析版) 题型:实验题
(13分)某校化学兴趣小组对课本实验结论“葡萄糖与新制氢氧化铜共热生成红色的Cu2O沉淀”提出质疑,认为红色沉淀不一定就是氧化亚铜。为了确定红色沉淀的成分,开展了相关探究。
[一]提出猜想,请你完成猜想2、3。
猜想1、红色沉淀可能是Cu;
猜想2、 ;
猜想3、 。
[二]查阅资料:①Cu20属于碱性氧化物②Cu+在酸I生条件下能发生自身氧化还原反应
[三]制备红色沉淀:①制备氢氧化铜悬浊液②氢氧化铜悬浊液与葡萄糖共热③过滤、洗涤、低温烘干得红色粉末
[四]红色沉淀成分探究:该小组同学设计了三种方案:
方案Ⅰ:取该红色粉末溶于足量稀硝酸中,观察溶液颜色变化。
方案Ⅱ:取该红色粉末溶于足量稀硫酸中,观察是否有残渣。
方案Ⅲ:装置如图所示:(夹持仪器略去)
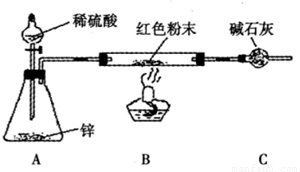
试回答下列问题:
(1)请分别评价方案I和方案Ⅱ是否合理(填“是”或“否”),并完成相关反应方程式:
方案I: ,写出Cu20与稀硝酸反应的化学方程式 ;
方案Ⅱ: ,写出反应的离子方程式 。
(2)实际上,方案Ⅲ的装置尚存在明显的缺陷,应在A和B之问添加 。
(3)方案Ⅲ中,探究小组的同学在锥形瓶中加入少量硫酸铜溶液,其目的是 。[来源:学_科_网Z_X_X_K]
(4)方案Ⅲ中,若要测定红色粉末的成分,需要测定下列哪些物理量 (填序号)。
①反应前红色粉末与硬质玻璃管的总质量 ②实验前干燥管的质量 ③实验后干
燥管的质量 ④硬质玻璃管的质量 ⑤锌粒质量 ⑥稀硫酸的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
1(16分) 某化学兴趣小组利用下图I探究铜和浓 H2SO4 反应生成气体的性质,图II用来收集多瓶该气体,请回答下列问题。(已知:Cu +2H2SO4(浓)![]() CuSO4 + 2H2O + SO2↑)
CuSO4 + 2H2O + SO2↑)
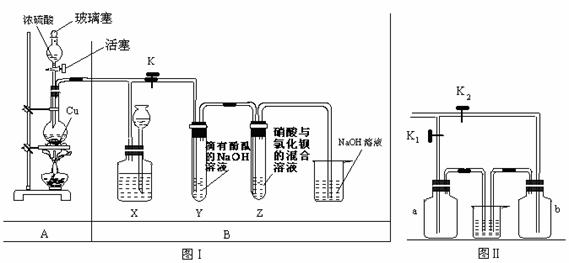
(1) 分液漏斗中盛有浓H2SO4,点燃酒精灯前打开分液漏斗的活塞,浓H2SO4不能顺利流下,可能的原因是________________________________________________。
(2) 装置X的作用是贮存气体,X中广口瓶内应盛放的液体最好是 ;
① Na2CO3 溶液 ② 酸性高锰酸钾 ③ Na2SO3 溶液 ④ 饱和NaHSO3 溶液
(3) 装置Y中产生的现象是 ,请用方程式解释产生该现象的原因 。
(4) 装置Z中产生的现象是 ,请用简要文字解释产生该现象的原因 。(提示:硝酸具有强氧化性)
(5) 实验需要收集多瓶反应产生的气体,在更换集气瓶时,为了减少气体逸散到空气中,将图I中的B部分更换为图II所示装置,可以用a、b 集气瓶交替收集二氧化硫气体,请回答:
① 检查集气瓶b 是否漏气的方法是______________________________________________________。
② 若只用集气瓶a 收集气体,在装置气密性良好,并加入药品后,准备制备并收集二氧化硫气体,下一步的操作是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com