

分析 (1)由方程式可知,增大压强,平衡正向移动,乙烯的转化率增大;
(2)Kp=$\frac{P({C}_{2}{H}_{5}OH)}{P({C}_{2}{H}_{4})P({H}_{2}O)^{\;}}$,利用三段法计算平衡分压带入表达式计算即可.
解答 解:(1)由图象可知在相同温度下由于乙烯转化率为P4>P3>P2>P1,由C2H4(g)+H2O(g)═C2H5OH(g)可知正反应为气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是P4>P3>P2>P1,
故答案为:P4>P3>P2>P1;
(2)C2H4(g)+H2O(g)═C2H5OH(g)
开始:1 1 0
转化:0.2 0.2 0.2
平衡:0.8 0.8 0.2
乙醇占$\frac{0.2}{0.8+0.8+0.2}$=$\frac{1}{9}$,乙烯和水各占$\frac{0.8}{0.8+0.8+0.2}$=$\frac{4}{9}$,则乙醇的分压为7.85MPa×$\frac{1}{9}$=0.87MPa,乙烯和水的分压为7.85MPa×$\frac{4}{9}$=3.49MPa,
所以Kp=$\frac{P({C}_{2}{H}_{5}OH)}{P({C}_{2}{H}_{4})P({H}_{2}O)^{\;}}$=$\frac{0.87MPa}{3.49MPa×3.49MPa}$=0.07(MPa)-1,
故答案为:0.07(MPa)-1.
点评 本题考查化学平衡的计算,为高考常见题型,题目涉及压强对平衡移动的影响、平衡常数的计算等知识,综合性非常强,属于中等难度较大,侧重于学生分析问题、解决问题、知识迁移能力的培养.


科目:高中化学 来源: 题型:解答题
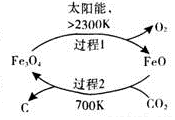 二氧化碳的回收利用是环保领域研究热点.
二氧化碳的回收利用是环保领域研究热点.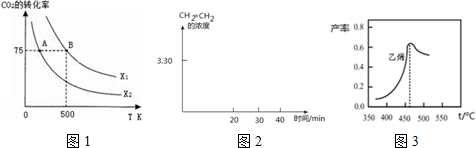
| 时间(min) 浓度(mol•L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| H2(g) | 6.00 | 5.40 | 5.10 | 9.00 | 8.40 | 8.40 |
| CO2(g) | 2.00 | 1.80 | 1.70 | 3.00 | 2.80 | 2.80 |
| CH2=CH2(g) | 0 | 0.10 | 0.15 | 3.20 | 3.30 | 3.30 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和反应的反应热测定需用温度计测量温度二次,分别为反应的起始温度和最高温度 | |
| B. | 用试纸检验气体时,可先把试纸用蒸馏水润湿,粘在玻璃棒一端,用玻璃棒把试纸放到盛待测气体的容器口附近 | |
| C. | 用剩的药品能否放回原瓶,应视具体情况而定 | |
| D. | 将铂丝放在盐酸中洗涤并灼烧为无色后,再蘸取待测物进行焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 操作 | |
| A | 证明某溶液中存在Fe2+ | 先加少量氯水,再滴加KSCN溶液,出现血红色 |
| B | 测定熔融苛性钠的导电性 | 在瓷坩埚中熔化氢氧化钠固体后进行测量 |
| C | 证明氯的非金属性大于碳 | 向碳酸钙中滴加盐酸,有气泡产生 |
| D | 制备氯化镁晶体 | 将MgCl2溶液在氯化氢的气流中蒸干 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
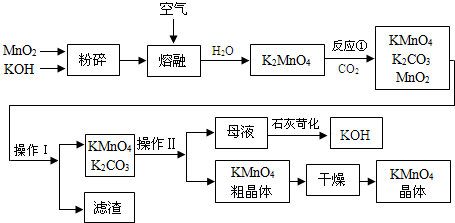
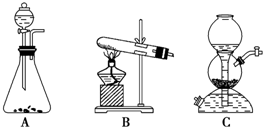
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应时间/min | n(SO2)/mol | n(O2)/mol |
| 0 | 0.10 | 0.060 |
| t1 | 0.012 | |
| t2 | 0.016 |
| A. | 反应在0~t1 min内的平均速率为v(SO3)=0.088/t1 mol•L-1•min-1 | |
| B. | 保持其他条件不变,起始时向容器中充入0.10molSO3和0.010 molO2,到达平衡时,n(SO2)=0.012 mol | |
| C. | 保持其他条件不变,升高温度,平衡时c(SO2)=0.0070mol•L-1,则反应的△H>0 | |
| D. | 相同温度下,起始时向容器中充入0.050molSO2和0.030molO2,达到平衡时SO2转化率大于88% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
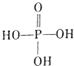
 .
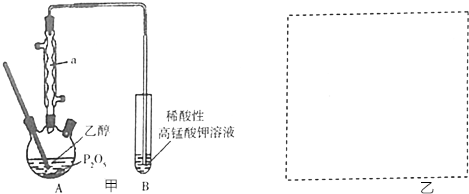
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com