
 化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.
化学能和电能的相互转化是能量转化的重要形式,电池在现代生活的很多方面得到广泛应用.分析 (1)没有外接电源且能自发进行氧化还原反应的装置为原电池,有外接电源的为电解池;
(2)甲装置为电解池,碳作阳极,阳极上氯离子放电;乙装置为原电池,铁易失电子作负极,碳作正极;
(3)正极氧气得到电子生成水;
(4)氧气在正极发生还原反应,锌在负极发生氧化反应,总反应为自发的氧化还原反应.
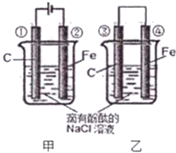
解答 解:(1)没有外接电源且能自发进行氧化还原反应的装置为原电池,原电池将化学能转化为电能,乙装置能自发进行氧化还原反应,符合原电池条件,所以乙属于原电池,甲有外接电源为电解池并且②的电极与负极相连为阴极,故答案为:乙;阴极;
(2)甲装置为电解池,碳作阳极,阳极①上氯离子放电生成氯气,电极反应式为2Cl--2e-═Cl2↑,乙装置为原电池,铁易失电子作负极,碳作正极,所以④电极上电极反应式为:Fe-2e-═Fe2+,故答案为:2Cl--2e-═Cl2↑,Fe-2e-═Fe2+;
(3)正极氧气得到电子生成水,电极方程式为O2+4e-+4H+=2H2O,故答案为:O2+4e-+4H+=2H2O;
(4)氧气在正极发生还原反应,电极反应式为:O2+4H++4e-═2H2O,锌在负极发生氧化反应,反应为:2Zn-4e-═2Zn2+,总反应为O2+4H++2Zn═2Zn2++2H2O,故答案为:O2+4H++2Zn═2Zn2++2H2O.
点评 本题考查了原电池和电解池原理,根据是否有外接电源判断原电池和电解池,再结合各个电极上发生的反应来分析解答,题目难度不大.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:解答题

| 开始沉淀时的pH | 完全沉淀时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Y3+ | 6.0 | 8.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙酸的结构式:CH3COOH | ||
| C. | 2-丁烯的键线式: | D. | 乙醇分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 下列叙述中正确的是( )
下列叙述中正确的是( )| A. | 该分子中所有原子共面 | |
| B. | 该分子可与FeCl3溶液反应呈紫色 | |
| C. | 1mol该物质最多可与4molH2发生反应 | |
| D. | 1mol该分子最多可与4mol溴发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
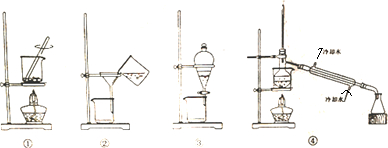
| A. | 装置①将海带灼烧成灰 | B. | 装置②过滤含I-的溶液 | ||
| C. | 装置③放出碘的CCl4溶液 | D. | 装置④分离碘并回收CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | H3PO2的电离方程式为:H3PO2?H2PO2-+H+;电离常数Ka≈10-5 | |
| B. | B点溶液中存在关系:2c(H+)+c(H3PO2)=2c(OH-)+c(H2PO2-) | |
| C. | 图2中的a点对应为 图1中的B点 | |
| D. | D点时,溶液中微粒浓度大小关系为:c(Na+)>c(H2PO2-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷,
2,2,4,5,7,7-六甲基-3,3,4-乙基辛烷, 下列各物质:与麻黄素互为同分异构体的是DE(填字母)
下列各物质:与麻黄素互为同分异构体的是DE(填字母)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com