
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是 ( )
A.电解饱和食盐水,阳极产生22.4 L气体时,电路中通过的电子数目为2NA
B.a g某气体含分子数为b,c g该气体在标准状况下的体积为![]() L
L
C.含有氢原子数为0.4NA的CH3OH分子中含有的共价键数目为0.5NA
D.常温下,1.0 L pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA
【答案】A
【解析】
根据题中阿伏加德罗常数可知,本题考查阿伏加德罗常数的计算,运用![]() 分析。
分析。
A.阳极产生气体的状态不明确,故22.4L气体的物质的量无法计算,则电路中通过的电子的数目无法计算,A项错误;
B.由于ag某气体含分子数为b,设cg该气体的分子个数为N,则有![]() 个,则气体的
个,则气体的![]() ,在标况下的气体体积
,在标况下的气体体积![]() ,B项正确;
,B项正确;
C. CH3OH分子中含4个H原子,含5个共价键,故当含有氢原子数为0.4NA时,含有的共价键为0.5NA,C项正确;
D.常温下,pH=13的氢氧化钡溶液中,氢离子浓度为1013mol/L,根据水的离子积可知氢氧根浓度![]() ,则1L溶液中含有的氢氧根的物质的量为0.1mol,个数为0.1NA个,D项正确。
,则1L溶液中含有的氢氧根的物质的量为0.1mol,个数为0.1NA个,D项正确。
答案选A。


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:
【题目】如图所示,将锌片和铜片按不同方式插入稀硫酸中,下列说法正确的是( )

A. 甲中电子经导线从铜片流向锌片
B. 两烧杯中锌片上均发生还原反应
C. 两烧杯中铜片表面均无气泡产生
D. 一段时间后,两烧杯中溶液的c(H+)均减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示实验合理的是( )

A.图甲证明非金属性强弱:S>C>Si
B.装置乙可用于检验有乙烯生成
C.图丙构成铜锌原电池,产生持续稳定的电流
D.图丁可制备并收集NO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的认识不正确的是
A. 油脂在空气中完全燃烧转化为水和二氧化碳
B. 蔗糖、麦芽糖的分子式都是C12H22O11,二者互为同分异构体
C. 在水溶液里,乙酸分子中的—CH3可以电离出H+
D. 在浓硫酸存在下,苯与浓硫酸共热生成硝基苯的反应属于取代反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为有效控制雾霾,各地积极采取措施改善大气质量,研究并有效控制空气中的氮氧化物、碳氧化物含量显得尤为重要。
Ⅰ.氮氧化物研究
(1)一定条件下,将2molNO与2molO2置于恒容密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g),下列各项能说明反应达到平衡状态的是____________。
2NO2(g),下列各项能说明反应达到平衡状态的是____________。
a.体系压强保持不变 b.混合气体密度保持不变
c.NO和O2的物质的量之比保持不变 d.每消耗2molNO同时生成2 molNO2
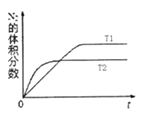
(2)汽车内燃机工作时会引起N2和O2的反应:N2+ O2![]() 2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ O2(g)
2NO,是导致汽车尾气中含有NO的原因之一。在T1、T2温度下,一定量的NO发生分解反应时N2的体积分数随时间变化如右图所示,根据图像判断反应N2(g)+ O2(g)![]() 2NO(g)的△H____0(填“>”或“<”)。
2NO(g)的△H____0(填“>”或“<”)。
(3)NOx是汽车尾气中的主要污染物之一。汽车发动机工作时会引发N2和O2反应,
其能量变化如图所示:
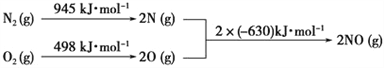
写出该反应的热化学方程式:________________________________。
Ⅱ.二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物。综合治理其污染是坏境化学当前的重要研究内容之一。
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(s)+O2(g)![]() 2SO3(g),某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
2SO3(g),某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示。根据图示回答下列问题:
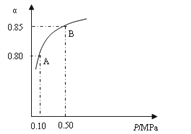
①将2.0 molSO2和1.0molO2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10MPa。该反应的平衡常数等于__________。
②平衡状态由A变到B时,平衡常数K(A)_______K(B)(填“>”、“<”或“=”)。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为__________(阿伏加德罗常数的值用NA表示),放出的热量为___________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:
(1)CH3COOH(l)+2O2(g)= 2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol
(2)C(s)+O2(g)= CO2(g) ΔH2=-393.5 kJ/mol
(3)H2(g)+![]() O2(g)= H2O(l) ΔH3=-285.8 kJ/mol
O2(g)= H2O(l) ΔH3=-285.8 kJ/mol
则反应2C(s)+2H2(g)+O2(g)= CH3COOH(l)的焓变为( ).
A.-488.3 kJ/molB.-244.15 kJ/molC.488.3 kJ/molD.244.15 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给下列有机物命名及写结构简式。
(1)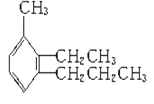 ____________________________________
____________________________________
(2)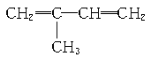 ____________________________________
____________________________________
(3)间甲基苯乙烯:_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)金刚烷的结构如图1所示,它可看作是由四个等同的六元环组成的空间构型。
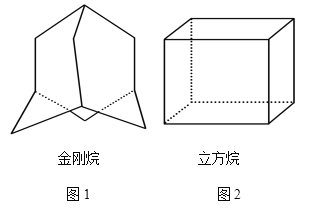
①金刚烷的分子式为________;
②根据中学学过的同分异构体判断规则,判断由溴原子取代分子中的氢原子形成的一溴代物有_____种。
(2)“立方烷”是一种新合成的烃,其分子为正方体结构,其碳架结构如图2所示。
①立方烷的分子式为______________________;
②该立方烷的二氯代物具有同分异构体的数目是_____________;
③将a g立方烷溶于b mL苯中,然后通入c L乙炔(标准状况下),所得混合物中碳的百分含量为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过以下反应可获得新型能源二甲醚(![]() )。下列说法不正确的是
)。下列说法不正确的是
①![]()
![]()
②![]()
![]()
③![]()
![]()
④![]()
![]()
A. 反应①、②为反应③提供原料气
B. 反应③也是![]() 资源化利用的方法之一
资源化利用的方法之一
C. 反应![]() 的
的![]()
D. 反应![]() 的
的![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com