
(9分)某二元酸H2A在水中的电离方程式:H2A==H++HA-;HA- H++A2-
H++A2-
试完成下列问题:
(1)Na2A溶液显 (填“酸性”、“中性”或“碱性”)。理由是
___________________________________________(用离子方程式表示)
(2)在0.1 mol/L的Na2A溶液中,下列离子浓度关系不正确的是 。
| A.c(A2-)+c(HA-)=0.1 mol/L |
| B.c(H+)=c(OH-)+c(HA-) |
| C.c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) |
| D.c(Na+)=2c(A2-)+2c(HA-) |
(1)碱性 A2-+H2O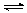 HA-+OH- (2)B、C
HA-+OH- (2)B、C
(3)c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
解析试题分析:(1)根据电离方程式可以看出H2A的第一步电离是完全的,第二步电离是不完全的,所以Na2A溶液可以水解呈碱性,水解方程式为A2-+H2O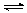 HA-+OH-。
HA-+OH-。
(2)由于H2A的第一步电离是完全的,所以溶液中不存在H2A分子,则A是正确的。根据电荷守恒c(H+)+ c(Na+)=c(OH-)+c(HA-)+2c(A2-),物料守恒c(Na+)=2c(A2-)+2c(HA-),可知c(OH-)= c(H+)+c(HA-),所以B、C错误,D正确。
(3)NaHA溶液中发生的电离反应有NaHA=Na++HA-,HA- H++A2-,HA-没有水解反应,所以溶液显酸性,溶液中的离子浓度大小关系是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)。
H++A2-,HA-没有水解反应,所以溶液显酸性,溶液中的离子浓度大小关系是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)。
考点:弱电解质的电离
点评:本题难度较大,主要考查学生分析问题的能力。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:桂壮红皮书·高中同步系列·活题巧解巧练·高二化学(上) 题型:013
已知某二元酸H2A在水溶液中的电离方程式:
H2A=H++HA-,HA-![]() H++A-
H++A-
测得25℃时0.1mol·L-1的H2A溶液中,c(H+)=0.11mol·L-1,则该条件下,HA-的电离度是
[ ]
|
A.1% |
B.9.1% |
|
C.10% |
D.55% |
查看答案和解析>>
科目:高中化学 来源:2014届山东省济宁市高二12月质量检测化学试卷(解析版) 题型:填空题
(9分)某二元酸H2A在水中的电离方程式:H2A==H++HA-;HA- H++A2-
H++A2-
试完成下列问题:
(1)Na2A溶液显 (填“酸性”、“中性”或“碱性”)。理由是
___________________________________________(用离子方程式表示)
(2)在0.1 mol/L的Na2A溶液中,下列离子浓度关系不正确的是 。
A.c(A2-)+c(HA-)=0.1 mol/L
B.c(H+)=c(OH-)+c(HA-)
C.c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-)
D.c(Na+)=2c(A2-)+2c(HA-)
(3) 0.1 mol/LNaHA溶液中各种离子浓度由大到小的顺序是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com