
| A. | 油脂 | B. | 蛋白质 | C. | 淀粉 | D. | 纤维素 |
科目:高中化学 来源: 题型:选择题
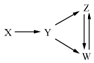 一定条件下,下列各组物质能一步实现如图所示转化关系的是( )
一定条件下,下列各组物质能一步实现如图所示转化关系的是( )| 选项 | X | Y | Z | W |
| A | Al | Al2O3 | NaAlO2 | Al(OH)3 |
| B | Fe2O3 | Fe | FeCl2 | FeCl3 |
| C | H2SO4 | SO2 | S | SO3 |
| D | NH3 | N2 | NO | NO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cl-、MnO4-、SO42- | B. | Na+、K+、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Na+、SO42-、H+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
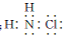 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | XX′n 属于活泼非金属单质 | |
| B. | ICl3 属于共价化合物 | |
| C. | 上述反应中HCl是还原产物 | |
| D. | ICl溶于水的反应:ICl+H2O=HIO+HCl 不属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和⑤ | B. | ②和③ | C. | ③⑤和⑥ | D. | ④和⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 200 mL 0.5mol/LNaCl溶液 | B. | 50 mL 0.3mol/LNa2SO4溶液 | ||
| C. | 150 mL 0.4mol/LNaOH | D. | 200mL0.15mol/LNa3PO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com