
|
金属钠的密度为0.97 g·cm3,水的密度为1 g·cm3.将一块金属钠投入水中,反应过程中可以观察到熔化成的闪亮小球,此时钠在水中的位置最合理的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
科目:高中化学 来源: 题型:038
钨酸钠(Na2WO4)和金属钨粉在隔绝空气的条件下加热得到一种具有金属光泽的、深色的、有导电性的固体——钨青铜,化学式NaxWO3,用X射线衍射法测得这种固体的立方晶胞的边长a=3.80×10-10 m,用比重法测得它的密度为ρ=7.36 g·cm-3,阿伏加德罗常数N=6.022×1023·mol-1。又已知用测定已知确切化学组成和晶系的纯净晶体的密度的方法测定阿伏加德罗常数的数值时,存在如下式:ρ·a3 ·N=Z·M(式中Z为常数,系1,2,3,……自然数,M为晶体的式量)
试回答下列问题:
(1)根据题意,从氧化还原反应角度判断钨青铜是钨酸钠的什么产物?
(2)根据(1)的结论和反应前后各元素守恒的原理,指出钨青铜分子组成的x的取值范围 。
(3)根据题中所给数据求这种固体的组成中的x值(2位有效数字),并给出计算过程。(已知:Na的相对原子质量为23.0,W的相对原子质量为183.9,O的相对原子质量为16.0)
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:022
试回答下列问题:
(1)根据题意,从氧化还原反应角度判断钨青铜是钨酸钠的什么产物?
(2)根据(1)的结论和反应前后各元素守恒的原理,指出钨青铜分子组成的x的取值范围 。
(3)根据题中所给数据求这种固体的组成中的x值(2位有效数字),并给出计算过程。(已知:Na的相对原子质量为23.0,W的相对原子质量为183.9,O的相对原子质量为16.0)
查看答案和解析>>
科目:高中化学 来源: 题型:043
钨酸钠(Na2WO4)和金属钨粉在隔绝空气的条件下加热得到一种具有金属光泽的、深色的、有导电性的固体——钨青铜,化学式NaxWO3,用X射线衍射法测得这种固体的立方晶胞的边长a=3.80×10-10 m,用比重法测得它的密度为ρ=7.36 g.(cm3)-1,阿伏加德罗常数N=6.022×1023.mol-1。又已知用测定已知确切化学组成和晶系的纯净晶体的密度的方法测定阿伏加德罗常数的数值时,存在如下式:ρ.a3.N=Z.M(式中Z为常数,系1,2,3,……自然数,M为晶体的式量)
试回答下列问题:
(1)根据题意,从氧化还原反应角度判断钨青铜是钨酸钠的什么产物?
(2)根据(1)的结论和反应前后各元素守恒的原理,指出钨青铜分子组成的x的取值范围 。
(3)根据题中所给数据求这种固体的组成中的x值(2位有效数字),并给出计算过程。(已知:Na的相对原子质量为23.0,W的相对原子质量为183.9,O的相对原子质量为16.0)
查看答案和解析>>
科目:高中化学 来源: 题型:
图6-4
(1)若用图6-4中所列仪器和导管组装实验装置,如果所制气体流向从左到右时,仪器和导管连接的顺序是________接________接________接________接________接________。(填编号)
(2)仪器连接好后进行实验时有下列操作:①在仪器C中装入
(3)这样制得的H2中含有什么气体杂质?应该怎样除去?
(4)若实验时消耗2.9 mL无水乙醇(密度为
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)若用下列仪器和导管(如下图所示)组装实验装置,如果所制气体流向从左到右时,则仪器与导管连接的顺序(填编号)是( )接( )接( )接( )接( )接( )。
(2)仪器连接好后进行实验时有下列操作:①在仪器F中注入适量的无水乙醇,在C中装入3克碎块状金属钠(足量),在E中注入过量的蒸馏水;②检查气密性;③待仪器C恢复到室温时,测定仪器D中水的体积;④慢慢开启仪器F的活塞,使乙醇逐滴滴下至不再发生反应时关闭活塞。正确的操作顺序是_____________(填序号)。
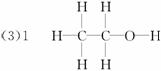
(3)若实验时消耗2.9 mL 的无水乙醇(密度为0.8 g·mL-1),测量排出的水的体积后折算成标准状况下的H2,体积为560 mL,根据以上数据推算出乙醇分子中可被置换的氢原子个数为_____________,结构式为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com