
NA代表阿伏伽德罗常数。已知C2H4和C3H6的混合物的质量为ag,则该混合物
A.所含共用电子对数目为(a/7+1)NA B.所含碳氢键数目为aNA/7
C.燃烧时消耗的O2一定是 33. 6a/ 14L D.所含原子总数为aNA/14
B
【解析】
试题分析: A、1个C2H4分子中含共用电子对数目为6,假设ag完全为C2H4,含共用电子对数目为3aNA/14, 1个C3H6分子中含共用电子对数目为9,假设ag完全为C3H6,含共用电子对数目为3aNA/14,则该混合物所含共用电子对数目为3aNA/14,错误;B、C2H4和C3H6的最简式均为CH2,1molCH2中含碳氢键数目为2NA,ag混合物中CH2的物质的量为a/14mol,含碳氢键数目为aNA/7,正确;C、没有明确温度和压强,无法确定消耗氧气的体积,错误;D、 C2H4和C3H6的最简式均为CH2,1molCH2中含原子数目为3NA,ag混合物中CH2的物质的量为a/14mol,含原子数目为3aNA/14,错误。
考点:考查阿伏伽德罗常数及相关物质的结构。


科目:高中化学 来源:2013-2014江西省抚州五校高三5月联考理综化学试卷(解析版) 题型:选择题
已知在比较酸的强弱时,必须考虑两方面:一是电离出氢离子的能力,二是溶剂接受氢离子的能力。比如HCl在水中是强酸,在冰醋酸中就是弱酸;而HAc在水中是弱酸,在液氨中却是强酸,就是因为接受氢离子的能力:NH3>H2O>HAc。下列关于酸性强弱的说法正确的是( )
A.在A溶剂中,甲的酸性大于乙;在B的溶剂中,甲的酸性可能小于乙
B.比较HCl、H2SO4、HClO4、HNO3酸性的强弱,用水肯定不可以,用冰醋酸可能可以
C.HNO3在HClO4中是酸,在H2SO4中可能是碱
D.比较HCN与HAc酸性的强弱,用水肯定可以,用液氨肯定也可以
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省南昌市高一文理分科测试化学试卷(解析版) 题型:填空题
(7分)
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有 和 。
(2)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法是:在100ml稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况):
时间/min | 1 | 2 | 3 | 4 | 5 |
体积/mL | 50 | 120 | 232 | 290 | 310 |
①哪一时间段反应速率最大_______(填“0~1 min”或“1~2 min”或“2~3 min”或“3~4 min”或“4~5min”)。
②2~3 min时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)为________。
③试分析1~3min时间段里,反应速率变大的主要原因 。
(3)对于容积固定的反应:N2(g)+3H2(g)  2NH3(g)(正反应放热),达到平衡的标志有___ 。
2NH3(g)(正反应放热),达到平衡的标志有___ 。
A N2、H2、NH3的百分含量不再变化 B 总压强不变
C N2、H2、NH3的分子数之比为1∶3∶2 D N2、H2、NH3的浓度相等
E.N2、H2不再起反应 F.v(N2)=v(H2)
G.混合气体的密度不变 H.混合气体的平均相对分子质量不变
I.正反应放出的热量等于逆反应吸收的热量
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省南昌市高一文理分科测试化学试卷(解析版) 题型:选择题
下列金属中,表面自然形成的氧化层能保护内层金属不被空气氧化的是
A.K B.Na C.Fe D.Al
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
某含Na+的溶液中可能含有NH4+、Fe3+、Br—、CO32—、I—、SO32—。取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无现象。为确定该溶液的组成,还需进行的实验有
A.取样,滴加硫氰化钾溶液
B.取样,加氯水和CCl4,振荡
C.取样,加足量盐酸加热,湿润的品红试纸检验气体
D.取样,加足量的熟石灰加热,湿润的红色石蕊试纸检验气体
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
如图所示,甲、乙、丙、丁分别代表Na2CO3、NaOH、NaHCO3、CO2四种物质,a、b、c、d、e、f分别表示两种物质间的转化关系。对于图中两种物质间的转化,通过一步反应就能实现的有

A.只有a、b、c、d B.只有b、c、d、e
C.只有c、d、e、f D.a、b、c、d、e、f
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省九江七校下学期期中联考高二化学试卷(解析版) 题型:实验题
(12分)乙醚极易挥发、微溶于水、是良好的有机溶剂。乙醇与浓硫酸的混合物在不同温度下反应能生成乙烯或乙醚。某实验小组用下图装置制取乙醚和乙烯。

1.制乙醚:在蒸馏烧瓶中先加入10 mL乙醇,慢慢加入10 mL浓硫酸,冷却,固定装置。加热到140℃时,打开分液漏斗活塞,继续滴加10 mL乙醇,并保持140℃,此时烧瓶c中收集到无色液体。
(1)Ⅰ和Ⅱ是反应发生装置,应该选择 (选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连。
(2)乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是
。
2.Ⅲ中水冷凝管的进水口是 (选答“a”或“b”)。冰盐水的作用是 。
3.有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险。该同学设
计了以下几种装置与导管d连接,你认为合理的是(选填编号) 。
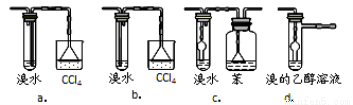
4.反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色。写出实验过程中有气体生成化学方程式(写两个方程式) ; 。
5.实验中收集到的乙醚产品中可能含有多种杂质。某同学设计了以下提纯方案:
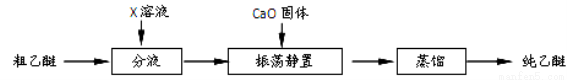
(1)分液步骤除去产品中的酸性杂质,则X可以是 。
(2)蒸馏操作可除去的杂质是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省九江七校下学期期中联考高二化学试卷(解析版) 题型:选择题
下列有机物中属于芳香烃的是( )
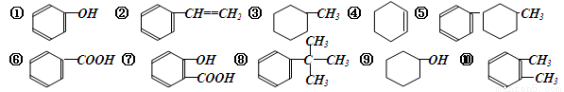
A.②⑧⑩ B.②⑤⑧⑩ C.③④⑧⑩ D.②③④⑤⑧⑩
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.蛋白质、纤维素、油脂、PVC、淀粉都是高分子化合物
B.油脂的皂化和硬化都是取代反应
C.饱和Na2SO4、CuSO4溶液均可用于蛋白质的盐析
D.红外光谱仪、核磁共振仪、质谱仪可用于有机化合物结构的分析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com