
用惰性电极电解尿素[CO(NH2)2]的碱性溶液制氢,装置如下图所示,电解池中的隔膜仅阻止气体通过。电解时总的化学方程式为:CO(NH2)2+2OH- CO32-+N2↑+3H2↑。
CO32-+N2↑+3H2↑。
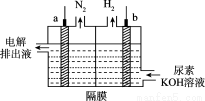
以下说法不正确的是( )
A.a为阳极,b为阴极
B.电解时,溶液中OH-向b极移动
C.阴极反应式:2H++2e-===H2↑
D.电解后,溶液pH减小
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
下列事实能说明HNO2为弱电解质的是( )
①0.1 mol/L HNO2溶液的pH=2.1
②常温下NaNO2溶液的pH>7
③用HNO2溶液做导电实验时,灯泡很暗
④HNO2溶液和KCl溶液不发生反应
⑤HNO2能与碳酸钠反应制CO2
⑥HNO2不稳定,易分解
A.①②③ B.①②④⑤ C.①②⑥ D.①②
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三12月月考化学试卷(解析版) 题型:选择题
工业上制备纯硅反应的热化学方程式为:SiCl4(g)+2H2(g) Si(s)+4HCl(g); △H = + QkJ/mol (Q>0),一定温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
Si(s)+4HCl(g); △H = + QkJ/mol (Q>0),一定温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 ( )
A. 反应过程中,若将硅移出体系,能提高SiCl4的转化率
B. 若反应开始时SiCl4为1mol,则达平衡时,吸收热量为QkJ
C. 反应至4min时,若HCl浓度为0.12mol/L,则H2的反应速率为0.03mol/(L min)
min)
D. 当反应吸收热量为0.025QkJ时,生成的HCl通入100mL 1mol/L的NaOH溶液恰好完全反应
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三12月月考化学试卷(解析版) 题型:选择题
25℃时,向25 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,滴定曲线如图所示,下列说法正确的是
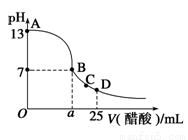
A.在A、B间任一点的溶液中一定都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.Ka(CH3COOH)=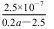
C.C点对应的溶液中,水电离出的H+浓度大于10-7 mol·L-1
D.D点对应的溶液中,存在如下关系:c(CH3COO-)-c(CH3COOH)=2c(H+)-c(OH-)
查看答案和解析>>
科目:高中化学 来源:2017届山东省德州市高三12月月考化学试卷(解析版) 题型:填空题
研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为______________________。利用反应6NO2+8NH3  7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是__________L。
7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是__________L。
2)已知:2SO2(g)+O2(g)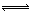 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)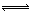 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)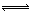 SO3(g)+NO(g)的ΔH=_________kJ·mol、1。
SO3(g)+NO(g)的ΔH=_________kJ·mol、1。
一定条件下,将NO2与SO2以体积比1︰2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1︰6,则平衡常数K=__________________。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)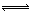 CH3OH(g)。
CH3OH(g)。
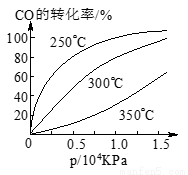
CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH___________0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________________________。
查看答案和解析>>
科目:高中化学 来源:2017届山东省德州市高三12月月考化学试卷(解析版) 题型:选择题
在一定温度下,固定体积为2L密闭容器中,发生反应:
2SO2(g)+O2(g)  2SO3(g ) ΔH <0,n(SO2)随时
2SO3(g ) ΔH <0,n(SO2)随时 间的变化如表:
间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是( )
A.当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B.用O2表示0~4 min 内该反应的平均速率为0.005 mol/(L·min)
内该反应的平均速率为0.005 mol/(L·min)
C. 平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
D.若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
查看答案和解析>>
科目:高中化学 来源:2017届山东省德州市高三12月月考化学试卷(解析版) 题型:选择题
高温下,某反应达到平衡,平衡常数K=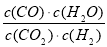 。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
。恒容时,温度升高,H2浓度减小。下列说法正确的是( )
A.该反应是焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为 CO+H2O  CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上学期阶段考二化学试卷(解析版) 题型:选择题
下列几种试剂不能把等物质的量浓度的Na2CO3、NaHCO3鉴别开的是( )
A.BaCl2溶液 B.澄清石灰水 C.稀盐酸 D.酚酞溶液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省慈溪市高二上学期期中化学试卷(解析版) 题型:选择题
25 ℃、101 kPa 下:①2Na(s)+ O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1
O2(g)=Na2O(s) ΔH1=-414 kJ·mol-1
②2Na(s)+O2(g)=Na2O2(s)ΔH2=-511 kJ·mol-1下列说法正确的是 ( )
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25 ℃、101 kPa下,Na2O2(s)+2Na(s)=2Na2O(s) ΔH=-317 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com