
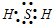 ,
,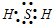 ;
;

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
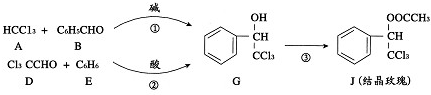
| KOH |
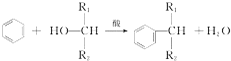 ,则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为
,则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 甲烷 | 乙烷 | 丁烷 | 戊烷 |
| 沸点 | -162℃ | -89℃ | -1℃ | +36℃ |
| A、约-40℃ |
| B、低于-162℃ |
| C、低于-89℃ |
| D、高于+36℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、容量瓶中含有少量蒸馏水,会导致所配标准溶液的浓度偏小 |
| B、配制溶液时,若在定容时仰视读数,会导致所配标准溶液的浓度偏大 |
| C、中和等体积、等物质的量的浓度的盐酸和醋酸所消耗的n(NaOH)相等 |
| D、25℃与60℃时,水的pH相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
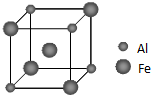 过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.
过渡元素铁可形成多种配合物,如:[Fe(CN)6]4-、Fe(SCN)3等.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
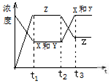 今有反应X(g)+Y(g)?3Z(g);△H<0若反应开始经t1秒后达到平衡,经t2秒后,由于反应条件的改变使平衡破坏,t3时又达到平衡,如图示,试分析,从t2到t3秒曲线变化的原因是( )
今有反应X(g)+Y(g)?3Z(g);△H<0若反应开始经t1秒后达到平衡,经t2秒后,由于反应条件的改变使平衡破坏,t3时又达到平衡,如图示,试分析,从t2到t3秒曲线变化的原因是( )| A、增加了反应体系的压强 |
| B、使用了催化剂 |
| C、升高了反应的温度 |
| D、增大了X和Y的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1个N≡N键断裂的同时,有3个H-H键形成 |
| B、1个N≡N键断裂的同时,有3个H-H键断裂 |
| C、1个N≡N键断裂的同时,有2个N-H键断裂 |
| D、1个N≡N键断裂的同时,有6个N-H键形成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com