
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量的氧化铁杂质。具体实验流程如下:
明矾石
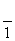

请回答下列问题:
(1)操作1所用到的玻璃仪器的名称是____________。
(2)由溶液3制取氢氧化铝的离子方程式为_______________________________
________________________________________________________________________。
(3)明矾石焙烧时产生SO2,请你写出能验证SO2具有还原性且实验现象明显的化学方程式:______________。
(4)请你写出验证溶液1中有NH 的实验过程:________________________。
的实验过程:________________________。
(5)实验室用Fe2O3与CO反应来制取单质Fe。
①请按气流由左到右的方向连接下列各装置,顺序为A→________。
②检查装置A气密性的方法是___________________________________________。
③在点燃B处的酒精灯前,应进行的操作是__________________。
④装置C的作用是________________。


解析 (1)操作1是过滤,过滤操作所需要的玻璃仪器为玻璃棒、烧杯和漏斗。(2)经氨水浸泡,过滤得到固体氢氧化铝和少量氧化铁固体,再加入试剂1氢氧化钠溶液并过滤,得到溶液3偏铝酸钠溶液,最后通入CO2得到氢氧化铝。(3)检验SO2的还原性方法较多,可以用氯水、溴水或酸性高锰酸钾溶液来检验SO2具有还原性。(4)检验NH 时,应先加入浓NaOH溶液,然后加热,再用湿润的红色石蕊试纸或蘸有浓盐酸的玻璃棒进行检验。(5)先用NaOH溶液除去CO中的CO2杂质,再通过碱石灰吸收水蒸气,再通过B中红热的氧化铁,再通过NaOH溶液洗气除去反应产生的CO2,最后点燃未反应的CO。
时,应先加入浓NaOH溶液,然后加热,再用湿润的红色石蕊试纸或蘸有浓盐酸的玻璃棒进行检验。(5)先用NaOH溶液除去CO中的CO2杂质,再通过碱石灰吸收水蒸气,再通过B中红热的氧化铁,再通过NaOH溶液洗气除去反应产生的CO2,最后点燃未反应的CO。
答案 (1)玻璃棒、烧杯和漏斗 (2)AlO +2H2O+CO2===Al(OH)3↓+HCO
+2H2O+CO2===Al(OH)3↓+HCO (3)SO2+Cl2+2H2O===H2SO4+2HCl(其他合理答案也可) (4)取少量溶液1,加入浓NaOH溶液后加热,有能使湿润的红色石蕊试纸变蓝的气体产生,证明有NH
(3)SO2+Cl2+2H2O===H2SO4+2HCl(其他合理答案也可) (4)取少量溶液1,加入浓NaOH溶液后加热,有能使湿润的红色石蕊试纸变蓝的气体产生,证明有NH (其他合理答案也可)
(其他合理答案也可)
(5)①E→B→C→D ②将导气管插入水槽中,关闭弹簧夹a和活塞b,微热圆底烧瓶,导管口有气泡产生,撤去热源,导管中形成一段稳定的水柱 ③检查CO的纯度 ④除去CO中的CO2,


科目:高中化学 来源: 题型:
Fe(OH)3胶体虽然是由FeCl3溶液制得,但两者是截然不同的两种物质。FeCl3溶液、Fe(OH)3胶体共同具备的性质是 ( )。
A.都呈透明的红褐色
B.分散质颗粒直径相同
C.都比较稳定,密封保存一段时间都不会产生沉淀
D.当有光线透过时,都能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时,难溶化合物的饱和溶液中存在着溶解平衡,例如:AgCl(s)Ag+(aq)+Cl-(aq),Ag2CrO4(s)2Ag+(aq)+CrO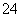 (aq),且Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12。
(aq),且Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12。
(1)若把足量的AgCl分别放入①100 mL蒸馏水,②100 mL 0.1 mol·L-1 NaCl溶液,③100 mL 0.1 mol·L-1 AlCl3溶液,④100 mL 0.1 mol·L-1 MgCl2溶液中,搅拌后在相同温度下Ag+浓度由大到小的顺序是____________________________(填序号)。
(2)现用0.001 mol·L-1 AgNO3溶液滴定0.001 mol·L-1 KCl和0.001 mol·L-1 K2CrO4的混合溶液,试通过计算回答:Cl-和CrO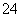 中哪种先沉淀?________。
中哪种先沉淀?________。
查看答案和解析>>
科目:高中化学 来源: 题型:
( 在5-氨基四唑(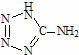 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊。
(1)基态Ga原子的电子排布式可表示为 ;
(2)5-氨基四唑中所含元素的电负性由大到小的顺序为 ;
在1mol 5-氨基四唑中含有的σ键的数目为 。
(3)叠氮酸钠(NaN3)是传统家用汽车安全气囊中使用的气体发生剂。
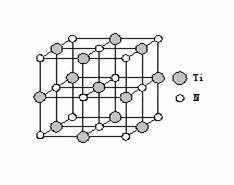
①叠氮酸钠(NaN3)中含有叠氮酸根离子(N3-),根据等电子体原理N3-的空间构型为 。②以四氯化钛、碳化钙、叠氮酸盐作原料,可以生成碳氮化钛化合物。其结构是用碳原子取代氮化钛晶胞(结构如上图示)顶点的氮原子,这种碳氮化钛化合物的化学式为 。
③与钛同周期的所有元素的基态原子中,未成对电子数与钛相同的元素有 。(填写元素符号)
④ [Ti(OH)2(H2O)4]2+中的化学键有 。
A.σ键 B.π键 C.离子键 D.配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气,某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气。供选用的实验试剂及装置如下图所示(部分导管、蒸馏水略)。
a.Na2O2 b.浓盐酸 c.碱石灰 d.NaOH溶液 e.淀粉KI溶液 f.CaCO3 g.石蕊溶液 h.饱和NaCl溶液

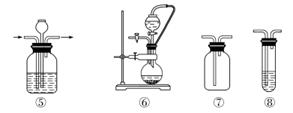
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式:__________________________
________________________________________________________________________
________________________________________________________________________。
(2)下表中的装置组合最合理的是__________(填字母,需考虑实验结束撤除装置时残留有害气体的处理)。
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为________________________________________________________________________。
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①________________________________________________________________________;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应4CO+2NO2N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最快的是( )
A.v(CO)=1.5 mol·L-1·min-1
B.v(NO2)=0.7 mol·L-1·min-1
C.v(N2)=0.4 mol·L-1·min-1
D.v(CO2)=1.1 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
催化反硝化法可用于治理水中硝酸盐的污染,H2能将NO 还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
还原为N2。25 ℃时,反应进行10 min,溶液的pH由7变为12,上述反应的离子方程式为________________________________________________________________________
________________________________________________________________________,
其平均反应速率v(NO )为________ mol·L-1·min-1。
)为________ mol·L-1·min-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下0.1 mol·L-1醋酸溶液的pH=a,下列能使溶液pH=(a+1)的措施是( )
A.将溶液稀释到原体积的10倍
B.加入适量的醋酸钠固体
C.加入等体积0.2 mol·L-1盐酸
D.提高溶液的温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com