
 当容器A中的反应开始后,若分别进行下列操作,请回答有关问题:
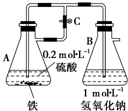
当容器A中的反应开始后,若分别进行下列操作,请回答有关问题:分析 由图可知,A中Fe与稀硫酸反应生成氢气,弹簧夹C打开,氢气进入B中;若关闭弹簧夹C,氢气将硫酸亚铁排入B中与NaOH反应生成氢氧化亚铁,氢气可排出B中空气,防止氢氧化亚铁被氧化,以此来解答.
解答 解:由图可知,A中Fe与稀硫酸反应生成氢气,弹簧夹C打开,氢气进入B中;若关闭弹簧夹C,氢气将硫酸亚铁排入B中与NaOH反应生成氢氧化亚铁,氢气可排出B中空气,防止氢氧化亚铁被氧化,
(1)若弹簧夹C打开,B容器中的现象是容器B中的导管口有气泡冒出,故答案为:容器B中的导管口有气泡冒出;
(2)若关闭弹簧夹C一会儿,容器A中的反应还在进行时,B容器中的现象是容器A中溶液进入容器B,有白色沉淀生成,沉淀迅速变为灰绿色,最后变为红褐色,B中发生2NaOH+FeSO4═Fe(OH)2↓+Na2SO4,4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:容器A中溶液进入容器B,有白色沉淀生成,沉淀迅速变为灰绿色,最后变为红褐色;2NaOH+FeSO4═Fe(OH)2↓+Na2SO4;4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(3)若先打开弹簧夹C一段时间,容器A中的反应还在进行时,再关闭弹簧夹C一会儿,B容器中的现象是开始时容器B中的导管口有气泡冒出,弹簧夹C关闭后容器A中溶液进入容器B,有白色沉淀生成,
故答案为:开始时容器B中的导管口有气泡冒出,弹簧夹C关闭后容器A中溶液进入容器B,有白色沉淀生成.
点评 本题考查氢氧化亚铁的制备实验,为高频考点,把握物质制备实验原理、实验装置的作用、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 加水时,平衡向逆反应方向移动 | |
| B. | 加入少量氢氧化钠固体,溶液中c(OH-)减小 | |
| C. | 通入少量HCl气体,平衡向正反应方向移动 | |
| D. | 加入少量NH4Cl固体,平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
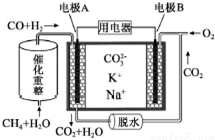
| A. | 电极A上H2参与的电极反应为:CO+H2+2CO32--4e-=3CO2+H2O | |
| B. | 理论上,A极每消耗1molH2,则消耗$\frac{1}{3}$molCH4 | |
| C. | 电池工作时,CO32-向电极A移动 | |
| D. | 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用加热灼烧的方法鉴别铁粉和炭粉 | |
| B. | 用酚酞溶液鉴别未知浓度的NaOH溶液和Na2CO3溶液 | |
| C. | 用丁达尔效应鉴别FeCl2溶液和FeCl3溶液 | |
| D. | 用氨水鉴别MgSO4溶液和Al2(SO4)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑ | B. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | ||
| C. | 2MgO$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ | D. | 2Al2O3$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 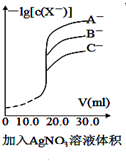 用硝酸银溶液滴定等浓度的A-、B-、C-的混合溶液(均可以与Ag+反应生成沉淀),由图可确定首先沉淀的是C- | |
| B. | 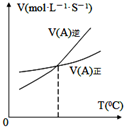 图表示反应中某反应物的正、逆反应速率随温度变化情况,由图可知该反应的正反应是吸热反应 | |
| C. | 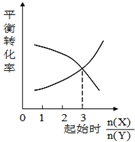 一定条件下,X和Y反应生成Z,由图1推出该反应的方程式可表示为:X+3Y?Z | |
| D. | 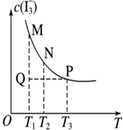 图表示溶液中反应:I2+I-?I3- 平衡c(I3-)随温度变化,反应速度V(正)M<V(逆)N |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com