
| A. | 硫化氢分子的电子式: | B. | S2-的结构示意图: | ||
| C. | HClO的结构式:H-O-Cl | D. | NH4Cl的电子式: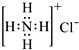 |
分析 A.H2S为共价化合物,硫原子与两个氢原子分别共用1对电子;
B.硫离子核内有16个质子,核外有18个电子;
C.次氯酸中心原子为氧原子,存在1个氧氯键和1个氢氧键;
D.氯化铵的电子式中氯离子的最外层电子式没有标出.
解答 解:A.H2S为共价化合物,硫原子与两个氢原子分别共用1对电子,电子式: ,故A错误;
,故A错误;
B.硫离子的核内有16个质子,故硫离子的结构示意图为: ,故B错误;
,故B错误;
C.次氯酸的中心原子是氧原子,结构式为H-O-Cl,故C正确;
D.NH4Cl为离子化合物,阴阳离子需要标出所带荷,铵根离子和氯离子还应该标出最外层电子,氯化铵正确的电子式为: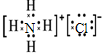 ,故D错误;
,故D错误;
故选:C.
点评 本题考查了常见化学用语的判断,题目难度中等,熟悉原子结构示意图、电子式、结构式的书写方法是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | X原子和Y原子最外层都只有一个电子 | |
| B. | X原子2p能级上有三个电子,Y原子的3p能级上有三个电子 | |
| C. | X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2 | |
| D. | X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将浓硝酸分别放在冷暗处和强光照射下,会发现强光照可以加快浓硝酸的分解 | |
| B. | 在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 | |
| C. | 将相同大小、形状的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 | |
| D. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,另一支试管不加;同时加热,产生氧气的快慢不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
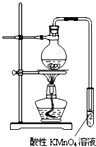 某学习小组探究溴乙烷的消去反应并验证产物.
某学习小组探究溴乙烷的消去反应并验证产物.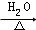 CH3CH2OH+NaBr.
CH3CH2OH+NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g OH-中含有的电子数为10 NA | |
| B. | 标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA | |
| C. | NA个Fe(OH)3胶体粒子的质量为107g | |
| D. | 44克14C16O2含氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④ | C. | ④ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gH2O含有的氢原子数目为NA | |
| B. | 常温常压下,22.4L CO2含有的分子数目为NA | |
| C. | 1mol钠在空气中充分燃烧失去的电子数目为NA | |
| D. | 1mol•L-1Na2SO4溶液中含有的钠离子数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com