
| A. | 氯化钙溶液 | B. | 澄清石灰水 | C. | 饱和碳酸钠溶液 | D. | 次氯酸钙溶液 |
分析 A.二氧化碳和氯化钙溶液不发生反应;
B.二氧化碳与过量氢氧化钙反应生成碳酸钙和水;
C.碳酸钠与二氧化碳和水反应生成溶解度较小的NaHCO3;
D.碳酸酸性强于次氯酸,二氧化碳与过量次氯酸钙反应生成次氯酸和碳酸钙.
解答 解:A.碳酸的酸性弱于盐酸,所以二氧化碳与氯化钙溶液不反应,不产生沉淀,故A正确;
B.二氧化碳与过量氢氧化钙反应生成碳酸钙和水,碳酸钙为白色沉淀,故B错误;
C.碳酸钠与二氧化碳和水反应,既消耗了水,且反应生成溶解度较小的NaHCO3,所以一定有沉淀析出,故C错误;
D.碳酸酸性强于次氯酸,二氧化碳与过量次氯酸钙反应生成次氯酸和碳酸钙,所以会产生白色沉淀,故D错误;
故选:A.
点评 本题考查了离子反应发生的条件,明确离子反应发生的条件、掌握常见元素化合物的化学性质是解题关键,题目难度不大.


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧元素的质量比为1:1 | B. | 质量之比为1:1 | ||
| C. | 原子总数之比为1:1 | D. | 硫元素的质量比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入的NaOH质量不一定最大 | |
| B. | 加入的Na2O2和Na2O的物质的量之比为1:1 | |
| C. | 制成饱和溶液后,4份溶液中所含NaOH质量相同 | |
| D. | 加入的NaOH、Na2O2、Na2O、Na的物质的量之比为2:1:1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Fe3+ | 2.7 | 3.7 |

| 实验 编号 | 待测溶液的体积(mL) | 滴定前标液的 体积读数(mL) | 滴定后标液的 体积读数(mL) |
| 1 | 20.00 | 1.20 | 21.22 |
| 2 | 20.00 | 2.21 | 22.19 |
| 3 | 20.00 | 1.50 | 23.48 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.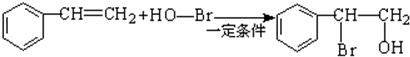 .
.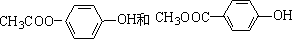 .
. )的合成线路:
)的合成线路: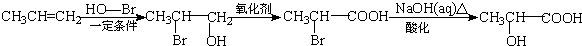 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验Ⅰ中溶液的酸性不断增强 | |
| B. | 两实验中生成等量Cl2时,转移电子数的物质的量相同 | |
| C. | 在实验Ⅰ的过程中,若NaHSO3初始量为3mol,当溶液中Cl-与Cl2的物质的量之比为5:2时,氧化产物为3.2mol | |
| D. | 试验Ⅱ反应结束后,加入碘化钾溶液,溶液呈蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com