
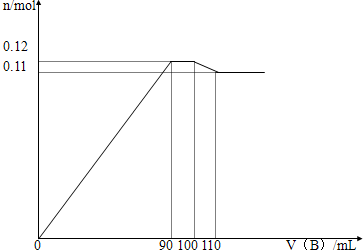
| 溶质 | c/mol?L-1 |
| Na2SO4 | |
| NaOH | |
| BaCl2 | |
| AlCl3 | |
| FeCl3 |
| 0.01mol |
| 0.01L |
| 0.01mol |
| 0.01L |
| 0.1mol |
| 0.1L |
| 0.01mol |
| 0.1L |
| 0.02mol |
| 0.1L |
| 溶质 | c/mol?L-1 |
| Na2SO4 | 1 |
| NaOH | 1 |
| BaCl2 | 1 |
| AlCl3 | 0.2 |
| FeCl3 | 0.1 |


科目:高中化学 来源: 题型:
| A、18 g D2O中含有的质子数目为10NA |
| B、7g乙烯和乙烷的混合气体中含有的氢原子数目为NA |
| C、标准状况下,22.4LCH3Cl中含有氯原子数目为NA |
| D、1 L0.5mol/LNa2CO3 溶液中含有的CO32-数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCO3-离子数略多于CO32-离子数 |
| B、HCO3-离子数等于CO32-离子数 |
| C、HCO3-离子数略少于CO32-离子数 |
| D、Na+离子数等于HCO3-离子数和CO32-离子数之和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该浓硝酸的物质的量浓度是14.0mol/L |
| B、得到12.7克沉淀时,加入的KOH溶液的体积是3.2L |
| C、该合金中铜与镁的物质的量之比是1:2 |
| D、NO2和N2O4的混合气体中,N2O4的体积分数是20% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入合金的质量可能为9.6g |
| B、参加反应的硝酸的物质的量为0.4mol |
| C、沉淀完全时消耗NaOH溶液体积为150mL |
| D、溶解合金时产生NO气体体积2.24L(STP) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、镀锌层破损后即对铁制品失去保护作用 |
| B、未通电前上述电镀装置可构成原电池,电镀过程是该原电池的充电过程 |
| C、电镀时保持电流恒定,升高温度不改变电解反应速率 |
| D、因部分电能转化为热能,电镀时通过的电量与锌的析出量无确定关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
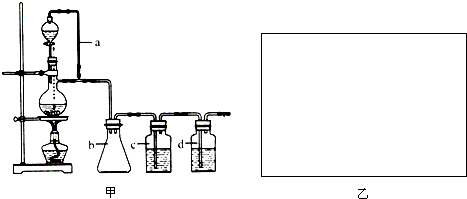
| 浓H2SO4 |
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com