
医学上常用酸性高锰酸钾溶液和草酸溶液的反应来测定血钙的含量。回答下列问题:

 H++
H++ 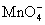 + H2C2O4==== CO2↑+ Mn2++
+ H2C2O4==== CO2↑+ Mn2++
(1)配平以上离子方程式,并在 中填上所需的微粒。
(2)该反应中的还原剂是 。
(3)反应转移了0.4 mol电子,则消耗KMnO4的物质的量为 mol。
(4)测定血钙的含量的方法:取2 mL血液用蒸馏水稀释后,向其中加入足量(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①稀硫酸溶解CaC2O4沉淀的化学方程式是 。
②溶解沉淀时 (“能”或“不能”)用稀盐酸,原因是 。
③若消耗了1.0×10-4mol·L-1的KMnO4溶液20.00 mL,则100 mL该血液中含钙
g。
【解析】(1)根据化合价升降总数相等,结合电荷守恒和元素守恒可配平该离子反应:6H++2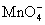 +5H2C2O4====10CO2↑+2Mn2++8H2O。
+5H2C2O4====10CO2↑+2Mn2++8H2O。
(2)反应中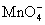 为氧化剂,H2C2O4为还原剂。
为氧化剂,H2C2O4为还原剂。
(3)根据反应中锰元素化合价变化,每有1 mol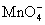 参加反应,则转移电子5 mol,因此反应转移0.4 mol电子,则消耗KMnO4的物质的量为0.08 mol。
参加反应,则转移电子5 mol,因此反应转移0.4 mol电子,则消耗KMnO4的物质的量为0.08 mol。
(4)CaC2O4不能用盐酸溶解,因为在酸性条件下,盐酸也可被KMnO4氧化,导致无法测定溶液中的H2C2O4。
根据题意,可得
5Ca2+→5CaC2O4→5H2C2O4→2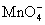
5 mol 2 mol
n(Ca2+) 1.0×10-4mol·L-1×20×10-3L
则n(Ca2+)=5.0×10-6mol。
100 mL该血液中含钙质量5.0×10-6mol×40 g·mol-1×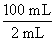 =0.01 g。
=0.01 g。
答案:(1)6 2 5 10 2 8 H2O
(2)H2C2O4
(3)0.08
(4)①CaC2O4+H2SO4====CaSO4+H2C2O4
②不能 KMnO4会氧化Cl-
③0.01


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案科目:高中化学 来源: 题型:
要检验溴乙烷中的溴原子,正确的实验方法是
A.加入氯水振荡,观察水层是否有红棕色出现
B.滴入AgNO3溶液,再加入稀硝酸,观察有无浅黄色沉淀生成
C.加入NaOH溶液共热,然后加入稀硝酸使溶液呈酸性,再滴入AgNO3溶液,观察有无浅黄色沉淀生成
D.加入NaOH溶液共热,然后加入AgNO3溶液,观察有无浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质递变规律不能用元素周期律解释的是( )
A. 非金属性:C>Si
B. 碱性:NaOH>Mg(OH)2
C. 酸性:H2SO3>H2CO3
D. 还原性:HI>HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:Fe2+能被稀硝酸氧化,反应方程式为:
3Fe(NO3)2 + 4HNO3(稀) → 3 Fe(NO3)3 + NO↑+ 2H2O
现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体的体积与剩余固体的质量如下表:
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 |
(1)放出4480 mL气体时,消耗金属的质量为_______g
(2)稀硝酸的浓度为_______ mol·L-1
(3)计算原混合物中铁和铜的物质的量比为
(4)加入400 mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一种酸性溶液中,可能存在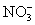 、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是( )
、I-、Cl-、Fe3+中的一种或几种离子,向该溶液中加入溴水,溴单质被还原,则以下的推测中不正确的是( )
A.一定有碘离子 B.可能含铁离子
C.可能有氯离子 D.不含硝酸根离子
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B(g) C(g)+D(g),5 min后达到平衡,已知该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
C(g)+D(g),5 min后达到平衡,已知该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
A.a=3 B.a=2
C.B的转化率为40% D.B的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
设反应①Fe(s)+CO2(g) FeO(s)+CO(g)
FeO(s)+CO(g)
ΔH=Q1的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
FeO(s)+H2(g) ΔH=Q2的平衡常数为K2,在不同温度下,K1、K2的值如下:
| 温度(T) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1 173 | 2.15 | 1.67 |
(1)从上表可推断,反应①是_______(填“放”或“吸”)热反应;
(2)现有反应③H2(g)+CO2(g) CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
CO(g)+H2O(g) ΔH=Q的平衡常数为K3。
Ⅰ.根据反应①与②推导出K1、K2、K3的关系式K3=______;可推断反应③是______(填“放”或“吸”)热反应。要使反应③在一定条件下建立的平衡右移,可采取的措施有____________________。
A.缩小容器体积 B.降低温度 C.使用合适的催化剂 D.设法减少CO的量
E.升高温度
Ⅱ.根据反应①与②推导出Q1、Q2、Q3的关系式Q3=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法摘自一些科普杂志或广告用语,你认为没有科学性错误的是( )
A.化学家采用玛瑙研钵摩擦固体反应物进行无溶剂合成,玛瑙的主要成分是硅酸盐
B.夏天到了,游客佩戴由添加氧化亚铜的二氧化硅玻璃制作的变色眼镜来保护眼睛
C.“白雪牌”漂粉精,令所有化学物质黯然失“色”,没有最白,只有更白
D.硅的提纯与应用,促进了半导体元件与集成芯片产业的发展,可以说“硅是信息技术革命的催化剂”
查看答案和解析>>
科目:高中化学 来源: 题型:
我国稀土资源丰富,下列有关稀土元素14462Sm与15062Sm的说法正确的是 ( )
A.14462Sm与15062Sm互为同位素
B.14462Sm与15062Sm的质量数相同
C.14462Sm与15062Sm是同一种核素
D.14462Sm与15062Sm的核外电子数和中子数均为62
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com