
分析 (1)A是一种正盐,E是强酸,由转化关系可知,中学化学中N、S元素化合物符合转化,当甲无论是强酸或强碱,A、B、C、D、E均为同种元素对应的不同的化合物,可推知A为(NH4)2S;
(2)当甲是稀盐酸溶液时,B为具有臭鸡蛋气味的气体,则B为H2S、C为SO2、D为SO3,E为H2SO4;
①二氧化硫与硫化氢反应生成硫与水;
②硫酸完全反应,发生反应:Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O,Zn+H2SO4=ZnSO4+H2↑,结合方程式计算;
(3)当甲是浓氢氧化钠溶液时,B为易液化的气体可作制冷剂,则B为NH3、C为NO、D为NO2、E为HNO3.
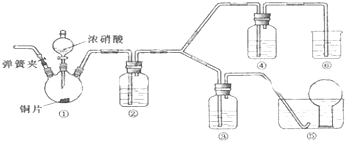
①在浓的硝酸溶液中放入过量的铜片,则反应将要结束时,为Cu与稀硝酸反应生成硝酸铜、NO与水;
②假定全部为二氧化氮,剩余气体体积为$\frac{1}{3}$×12mL=4mL,大于实际剩余2mL气体,则说明剩余气体为NO或氧气.
若剩余气体为氧气,根据4NO2+O2+2H2O=4HNO3,求NO2的体积,总体积减去NO2的体积可得混合气体中氧气的体积;
若剩余气体为NO,先根据3NO2+H2O=2HNO3+2NO求出过量的NO2,然后根据4NO2+O2+2H2O=4HNO3求出O2的体积.
解答 解:(1)A是一种正盐,E是强酸,由转化关系可知,中学化学中N、S元素化合物符合转化,当甲无论是强酸或强碱,A、B、C、D、E均为同种元素对应的不同的化合物,可推知A为(NH4)2S,
故答案为:(NH4)2S;
(2)当甲是稀盐酸溶液时,B为具有臭鸡蛋气味的气体,则B为H2S、C为SO2、D为SO3,E为H2SO4,则:
①B与C的反应方程式为:2H2S+SO2=3S↓+2H2O,
故答案为:2H2S+SO2=3S↓+2H2O;
②一定质量的Zn与100mL 12.0mol/L的H2SO4的浓溶液充分反应,反应后称量剩余锌发现质量减少了65.0g,则参加反应Zn的物质的量为1mol,H2SO4的物质的量为0.1L×12mol/L=1.2mol,
由于硫酸都没有剩余,设与浓硫酸反应的Zn为xmol,与稀硫酸反应的Zn为ymol,则:
Zn+2H2SO4(浓)=ZnSO4+SO2↑+H2O
x 2x x x
Zn+H2SO4=ZnSO4+H2↑
y y y
由题意可知:$\left\{\begin{array}{l}{x+y=1}\\{2x+y=1.2}\end{array}\right.$,解得x=0.2 y=0.8,
故将反应后的溶液稀释至1L,此时溶液中c(SO42-)=$\frac{0.2mol+0.8mol}{1L}$=1mol/L,产生SO2体积(标准状况下)=0.2mol×22.4L/mol=4.48L,
故答案为:1;4.48;
(3)当甲是浓氢氧化钠溶液时,B为易液化的气体可作制冷剂,则B为NH3、C为NO、D为NO2、E为HNO3.
①由上述分析可知C是NO,在浓的E溶液中放入过量的铜片,则反应将要结束时,为Cu与稀硝酸反应,离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:NO;3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
②假定全部为二氧化氮,剩余气体体积为$\frac{1}{3}$×12mL=4mL,大于实际剩余2mL气体,则说明剩余气体为NO或氧气.
若剩余气体为氧气,则参加反应的气体为12mL-2mL=10mL,根据4NO2+O2+2H2O=4HNO3,可知参加此反应的NO2的体积为10mL×$\frac{4}{5}$=8mL,参加反应的O2的体积为10mL-8mL=2mL,原混合气体中O2的体积为2mL+2mL=4mL;
若剩余气体为NO气体,根据3NO2+H2O=2HNO3+NO,可知过量的NO2为3×2mL=6mL,反应4NO2+O2+2H2O=4HNO3消耗的气体总体积为12mL-6mL=6mL,则反应消耗的氧气为6mL×$\frac{1}{5}$=1.2mL,
故答案为:4或1.2.
点评 本题考查无机物推断,属于开放性题目,需要学生熟练掌握元素化合物知识,侧重考查化学用语与化学计算,(3)中关键是分析剩余气体的成分,进行讨论计算.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 石灰乳中通入Cl2制漂白精的离子反应方程式为:4OH-+2Ca2++2Cl2═2Cl-+Ca(ClO)2↓+2H2O | |
| B. | NaHCO3中滴入少量Ba(OH)2溶液,其离子方程式正确的是:H++CO32-+Ba2++OH-═BaCO3↓+H2O | |
| C. | 1.0 mol•L-1的KNO3溶液中H+、Fe2+、Cl-、SO42- 能大量共存 | |
| D. | pH=12的溶液中K+、Na+、CH3COO-、Br-能大量共存 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
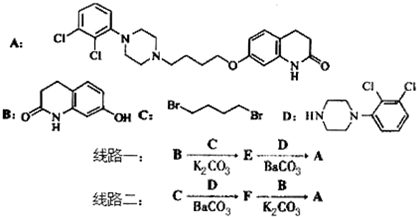
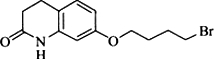 ,其含氧官能团有肽键、醚键(写名称).
,其含氧官能团有肽键、醚键(写名称).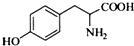 、
、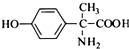 .
.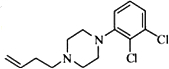 .
.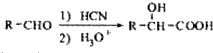 写出由C制备化合物
写出由C制备化合物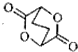
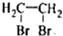
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 检验蔗糖水解产物中的葡萄糖 | 取1mL 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液,加入几滴新制Cu(OH)2悬浊液,加热 |
| B | 除去乙烷中混有的少量乙烯 | 将混合气体通入足量酸性KMnO4溶液中 |
| C | 验证Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2mL 1mol•L-1 NaOH溶液中加入几滴1mol•L-1 MgCl2溶液,生成白色沉淀,再加入几滴1mol•L-1 FeCl3溶液 |
| D | 硅酸胶体的制备 | 向Na2SiO3溶液(饱和溶液1:2用水稀释)中加入几滴酚酞,再逐滴滴入盐酸,边加边振荡,至溶液红色变浅并接近消失 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨烯弹性气凝胶可用作处理海上原油泄漏的吸油材料 | |
| B. | 压减燃煤、严格控车、调整产业是治理雾霾有效措施 | |
| C. | 绚丽缤纷彩色的烟花中添加了含钾、钠、铁、铜等金属化合物 | |
| D. | 使用该分子催化剂可将一次能源太阳能直接转化成二次能源,例如电能、氢能 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
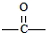 +R-Mgx→
+R-Mgx→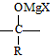 $\stackrel{H+/H_{2}O}{→}$
$\stackrel{H+/H_{2}O}{→}$ (R代表烃基,X代表卤素原子)
(R代表烃基,X代表卤素原子)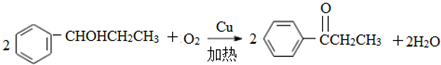 .
.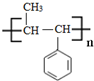 .
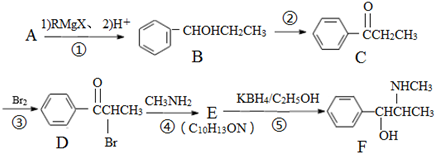
.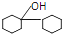 是合成感冒药物中的一种原料,实验室可用环己烯按以下合成路线合成该有机物:
是合成感冒药物中的一种原料,实验室可用环己烯按以下合成路线合成该有机物: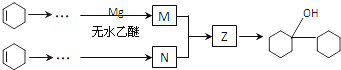
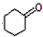 ;Z
;Z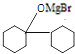 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,有机物(CH3)2CHCH(CH2CH3)(CH2CH2CH3)的命名为:2-甲基-3-丙基戊烷 | |
| B. | 已知C-C键可以绕键轴自由旋转,结构简式为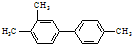 分子中至少有7个碳原子处于同一直线上 分子中至少有7个碳原子处于同一直线上 | |
| C. | 肌醇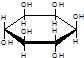 与葡萄糖 与葡萄糖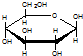 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 的元素组成相同,化学式均为C6H12O6,满足Cm(H2O)n,因此,均属于糖类化合物 | |
| D. | 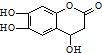 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H6O6Na4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com