
【题目】连二亚硫酸钠(Na2S2O4)又称保险粉,是白色砂状或淡黄色粉末固体,己知连二业硫酸钠在碱性条件下较稳定,易被空气氧化,不溶于甲醇,遇水迅速分解,某同学设计利用如下图所示的实验装置制备一定量的连二亚硫酸钠,装置C中的试剂为甲酸钠(HCOONa)、NaOH 的甲醇溶液,回答下列问题:
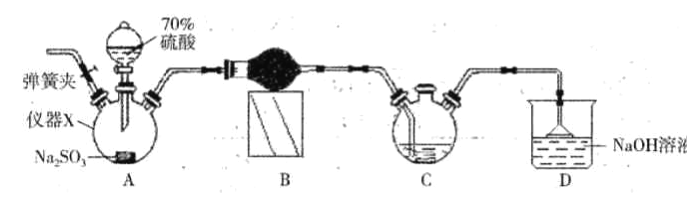
(1)仪器X的名称是_____。装置B中的球形干燥管中盛装的试剂是_______。
(2)装置D的作用是___________。实验时需要将C中温度控制在70-75℃,最好的控制方法是__________。
(3)实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是______。实验过程中装置C 中除有气体产生外,还能观察到的实验现象为____________。
(4)有同学通过仔细思考后认为,还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是______。为得到较纯的连二亚硫酸钠,需要对在过滤时得到的连二亚硫酸钠进行洗涤,洗涤的方法是_________。
(5)若实验中所用Na2SO3的质量为12.6g (硫酸是过量的),最终得到m g干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为_____________。
【答案】 三颈烧瓶 无水CaCl2或P2O5 吸收过量的SO2,防止其污染空气 水浴加热 排出装置中的O2,避免其氧化连二亚硫酸钠 有(白色或淡黄色)固体生成 吸收水蒸气 在无氧环境中,向漏斗中加入甲醇至浸没晶体,待甲醇顺利流下后,重复2-3次 m/8.7×100%
【解析】(1)根据构造可判断仪器X的名称是三颈烧瓶。装置B用来干燥二氧化硫,二氧化硫是酸性氧化物,因此其中的球形干燥管中盛装的试剂是无水CaCl2或P2O5。(2)二氧化硫属于大气污染物,装置D的作用是吸收过量的SO2,防止其污染空气。实验时需要将C中温度控制在70~75℃,最好的控制方法是水浴加热。(3)连二亚硫酸钠易被空气氧化,装置中含有空气,因此实验开始时先打开装置A中的弹簧夹通入一段时间N2的目的是排出装置中的O2,避免其氧化连二亚硫酸钠。由于连二亚硫酸钠是白色砂状或淡黄色粉末固体,因此实验过程中装置C 中除有气体产生外,还能观察到的实验现象为有白色或淡黄色固体生成。(4)由于D装置中的水蒸气有可能进入到C装置中,因此还应在C、D 之间添加一个装置,才能确保C中生成能稳定存在的连二亚硫酸钠,则该装置应具有的功能是吸收水蒸气。由于产品易被氧化,不溶于甲醇,遇水迅速分解,所以洗涤的方法是在无氧环境中,向漏斗中加入甲醇至浸没晶体,待甲醇顺利流下后,重复2~3次。(5)Na2SO3的质量为12.6g,物质的量是0.1mol,根据S原子守恒可知理论上得到产品质量是0.05mol×174g/mol=8.7g,最终得到mg干燥的连二亚硫酸钠,则连二亚硫酸钠的产率为m/8.7×100%。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】日常生活中常用到许多化学知识,下列说法不正确的是( )
A. 热的纯碱(Na2CO3)水溶液(显碱性)可清洗油污
B. 将含有甲醇的工业酒精兑制成饮用白酒
C. 不能用苏丹红(色素)作食品的着色剂
D. 蚕丝和羊毛都属于动物纤维,又称蛋白纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是有关SO2、Cl2的性质实验.
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质. 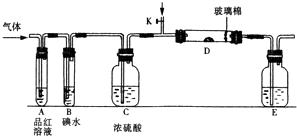
若从左端分别通入SO2和Cl2 , 装置A中观察到的现象是否相同?(填“相同”或“不相同”); 若装置D中装的是五氧化二钒(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为E中盛有溶液.
(2)若装置B中装有5.0mL 1.0×10﹣3mol/L碘水,当通入足量Cl2完全反应后,共转移了5.0×10﹣5mol电子,该反应的化学方程式为 .
(3)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母) , 则可以看到白色沉淀产生.
A.氨水
B.稀盐酸
C.稀硝酸
D.氯化钙.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示几种中学常见物质之间的相互转化关系(图中部分条件或产物已省略),其中B为黑色的非金属固体单质,D可使品红溶液褪色,E在通常状况下是无色无味的液体,I在通常状况下是无色气体,G是淡黄色的固体化合物,H是黑色晶体. 
请回答下列问题:
(1)单质F的组成元素在周期表中的位置是(指明周期和族),G的电子式为 , 化合物J的俗名 .
(2)金属Al和H的混合物俗称
(3)镁条能在气体C中燃烧得到两种固体,其化学式分别是、;
(4)写出上图中下列反应的化学方程式:
①;
③;
(5)向上图中的反应⑤得到的M、N混合液中通入H2S气体,溶液变浑浊,酸性增强.请写出该过程发生反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境污染已成为人类社会面临的重大威胁,下列对应关系不正确的是( )
A. 酸雨——二氧化硫 B. 温室效应——二氧化碳
C. 光化学烟雾——二氧化氮 D. 白色污染——二氧化硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置进行实验,并回答下列问题(提示:装置A为B的化学电源)
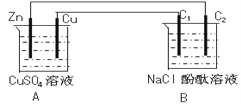
(1)锌极为__________极,电极反应式为__________________________________
(2)石墨棒C1为______极,电极反应式为__________________________________,石墨棒C2附近发生的实验现象为__________________________________
(3)当C2极析出224mL气体(标准状态)时,锌的质量减少_________g;
(4)此时装置B中OH-的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.NaCl 溶液在电流的作用下电离成 Na+和 Cl-
B.由非金属元素组成的化合物一定是共价化合物
C.离子化合物中可能含有非极性键或极性键
D.分子晶体中,分子间作用力越大,分子越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年全国两会普及使用了“石头纸”,这是以碳酸钙为主料(内层)、聚乙烯等高分子材料为辅料(双外层)制成的,有关“石头纸”的说法错误的是( )
A.不易燃烧B.有利于保护森林C.防油不防水D.不易降解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图1是部分短周期元素的常见化合价与原子序数的关系图: 
(1)画出元素F的原子结构示意图 .
(2)从上述元素中选取两种元素形成既含离子键又含共价键的化合物,该化合物的电子式为 .
(3)这些元素中,最高价氧化物对应的水化物中酸性最强的化合物分子式为 .
(4)C、D、G对应的简单离子半径由小到大的顺序是 . (用离子符号回答)
(5)某同学设计实验装置如图2,证明A、B、F的非金属性强弱关系:
①溶液a和溶液b分别为 , .
②溶液c中的离子反应方程式为 .
③请从原子结构的角度解释非金属性B>A的原因
(6)将1mol D2C2投入200mL 3mol/L EH3溶液中,
①转移电子的物质的量为 .
②用一个化学反应方程式表示该反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com