
【题目】下图是实验室硫酸试剂标签上的部分内容,据此下列说法正确的是( )

A. 该硫酸的物质的量浓度为9.2mol/L
B. 1molAl与足量的该硫酸反应产生3g氢气
C. 配制500mL4.6 mol/L的稀硫酸需取该硫酸125mL
D. 将该硫酸加水配成质量分数49%的溶液时其物质的量浓度等于9.2mol/L
【答案】C
【解析】A.根据c=![]() 计算浓硫酸的物质的量浓度;
计算浓硫酸的物质的量浓度;
B. 铝与浓硫酸常温下发生钝化,加热时生成二氧化硫和硫酸铝;
C.根据溶液稀释前后溶质物质的量不变计算所需浓硫酸的体积;
D.硫酸与等质量的水混合,混合后溶液的质量为原硫酸的2倍,稀释后溶液的密度减小,故稀释后所得溶液的体积大于原硫酸体积的2倍,根据稀释定律判断。
A.该浓H2SO4的物质的量浓度为:c=![]() =
=![]() mol/L=18.4mol/L,所以A选项是错误的;
mol/L=18.4mol/L,所以A选项是错误的;
B. 铝与浓硫酸常温下发生钝化,加热时生成二氧化硫和硫酸铝,不能生成氢气,故B错误;
C.根据稀释定律,稀释前后溶质的物质的量不变,设浓硫酸的体积为xmL,则xmL×18.4mol/L=500mL×4.6mol/L,计算得出:x=125,所以应量取的浓硫酸体积是125mL,所以C选项是正确的;
D.硫酸与等质量的水混合,混合后溶液的质量为原硫酸的2倍,稀释后溶液的密度减小,故稀释后所得溶液的体积大于原硫酸体积的2倍,则稀释后所得溶液的浓度小于9.2mol/L,故D错误;
所以C选项是正确的。


科目:高中化学 来源: 题型:
【题目】某强酸性溶液X可能含有Fe2+、A13+、NH4+、CO32-、SO32-、SO42-、C1-中的若干种,现取X溶液进行连续实验,实验过程及产物如图.说法正确的是

A. X中肯定存在Fe2+、A13+、NH4+、SO42- B. X中不能确定的离子是 A13+和C1-
C. 沉淀I一定是Al(OH)3 D. 溶液E和气体F不能发生化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是宝贵的资源宝库,目前氯碱工业、海水提镁、海水提溴为人类提供了大量工业原料。下图是海水综合利用的部分流程图,据图回答问题:
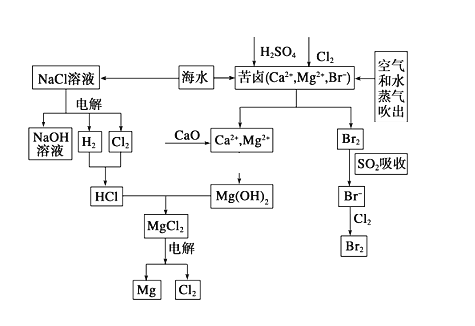
(1)由海水晒制的粗盐中含有Ca2+、Mg2+、SO42-等离子,为除去这些离子,所加试剂及其先后顺序为(写化学式) ______________________。
(2)①电解饱和食盐水的化学反应方程式为______________。
②制取MgCl2的过程中涉及反应:MgCl2·6H2O![]() MgCl2+6H2O,该反应要在HCl气氛中进行,原因是_______________。
MgCl2+6H2O,该反应要在HCl气氛中进行,原因是_______________。
(3)苦卤中通入Cl2置换出Br2,吹出后用SO2吸收,写出用SO2吸收发生的离子方程式_________,由此判断Cl2、Br2、SO2的氧化性由强到弱的顺序为__________________。
(4)也有工艺是在吹出Br2后用碳酸钠溶液吸收,形成溴化钠和溴酸钠,同时有CO2放出。该反应的离子方程式是_____________;最后再用H2SO4处理得到Br2,之后加入CCl4进行Br2的萃取,最终用_____________方法得到单质Br2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素化学性质发生周期变化性质变化的根本原因是
A.元素的原子半径呈周期性的变化
B.元素的化合价呈现周期性变化
C.元素原子核外电子排布呈现周期性变化
D.元素的金属性和非金属性呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤气中主要的含硫杂质有H2S以及COS(有机硫),煤气燃烧后含硫杂质会转化成SO2从而引起大气污染,因此煤气中H2S的脱出程度已成为煤气洁净度的一个重要指标。请回答下列问题:
(1)脱除煤气中COS的方法有Br2的KOH溶液氧化法、H2还原法、水解法等。
①COS的分子结构与CO2相似,COS的结构式为___________。
②Br2的KOH溶液将COS氧化为硫酸盐的离子方程式为______________。
③已知:H2、COS、H2S、CO的燃烧热依次为285kJ/mol、299kJ/mol、586kJ/mol、283kJ/mol;H2还原COS发生的反应为H2(g)+COS(g)=H2S(g)+CO(g),该反应的ΔH=_________kJ/mol。
恒温恒容条件下,密闭容器中将气体按n(H2):n(COS)=2:1混合发生下列反应,下列事实能说明反应达到平衡状态的是_______(填字母)
a.混合气体的平均相对分子质量不再改变 b. n(H2)与n(COS)的比值不变
c.CO的体积分数不变 d.形成2 mol H-S键的同时形成1 mol H-H键
④用活性α-Al2O3催化COS水解反应为COS(g)+H2O(g)![]() CO2(g)+H2S(g) ΔH<0,相同流量且在催化剂表面停留相同时间时,不同温度下H2S的转化率(未达到平衡)如图所示
CO2(g)+H2S(g) ΔH<0,相同流量且在催化剂表面停留相同时间时,不同温度下H2S的转化率(未达到平衡)如图所示

由图可知,催化剂活性最大时对应的温度约为______,H2S的转化率在后期下降的原因是_______________________________________。
(2)煤气燃烧后含硫杂质转化成的SO2,可以被氨水吸收,已知25℃时,NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.3×10-2, Ka2=6.2×10-8.将SO2通入氨水中,当溶液呈中性时,溶液中的c(NH4+)/c(HSO3-)=_____________________.此时溶液中各离子浓度大小关系为:_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空。
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是________,只有还原性的是________,既有氧化性又有还原性的是________。
(2)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O ②NH3+NO→HNO2+H2O ③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是________。
(3)下列三个氧化还原反应中,氧化性最强的物质是________。
①2FeCl3+2KI===2FeCl2+2KCl+I2 ②2FeCl2+Cl2===2FeCl3
③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若溶质中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除单质外,还应用上述反应中的________作氧化剂。
(4)请配平以下化学方程式:___
![]() Al+
Al+![]() NaNO3+
NaNO3+![]() NaOH===
NaOH===![]() NaAlO2+
NaAlO2+![]() N2↑+
N2↑+![]() H2O
H2O
若反应过程中转移5 mol电子,则生成标准状况下N2的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的分类或变化说法正确的是
A. NaCl溶液是强电解质
B. 二氧化氮经加压凝成无色液体为物理变化
C. Na2OSiO2是硅酸盐,可溶于水
D. 溴水滴入植物油中褪色说明溴被植物油萃取出来
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com