
辉铜矿(主成份为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E.G为砖红色沉淀.
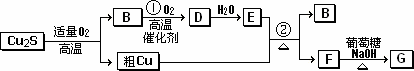
请回答下列问题:
(1)辉铜矿(Cu2S)通适量的空气冶炼金属铜的化学方程式________其中氧化剂为________.
(2)E的浓溶液与Cu发生反应②的化学方程式是________.
(3)利用电解可提纯粗,在该电解反应中阳极物质是________,电解质溶液是________;
(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿.对反应:14CuSO4+5FeS2+12H2O 7Cu2S+5FeSO4+12H2SO4被氧化的硫和被还原的硫的质量比为________;
7Cu2S+5FeSO4+12H2SO4被氧化的硫和被还原的硫的质量比为________;
科目:高中化学 来源: 题型:

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分) 辉铜矿(主成份为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E。G为砖红色沉淀。
请回答下列问题:
(1)辉铜矿(Cu2S)通适量的空气冶炼金属铜的化学方程式__________________________
______其中氧化剂为____________________。
(2)E的浓溶液与Cu发生反应②的化学方程式是 。
(3)利用电解可提纯粗,在该电解反应中阳极物质是 ,电解质溶液是 ;
(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿。对反应:14CuSO4+ 5FeS2 +12H2O==7Cu2S+5FeSO4+12H2SO4
被氧化的硫和被还原的硫的质量比为_________________________;
查看答案和解析>>
科目:高中化学 来源:2012届山西省康杰中学高三9月份月考化学试卷 题型:填空题
(14分)辉铜矿(主成份为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E。G为砖红色沉淀。
请回答下列问题:
(1)辉铜矿(Cu2S)通适量的空气冶炼金属铜的化学方程式__________________________
______其中氧化剂为____________________。
(2)E的浓溶液与Cu发生反应②的化学方程式是 。
(3)利用电解可提纯粗,在该电解反应中阳极物质是 ,电解质溶液是 ;
(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿。对反应:14CuSO4+ 5FeS2 +12H2O==7Cu2S+5FeSO4+12H2SO4
被氧化的硫和被还原的硫的质量比为_________________________;
查看答案和解析>>
科目:高中化学 来源:2012届浙江省浙南、浙北部分学校高三12月联考化学试卷 题型:填空题
(8分)辉铜矿(主成份为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E。G为砖红色沉淀。
请回答下列问题:
(1)辉铜矿(Cu2S)通 适量的空气冶炼金属铜的化学方程式__________________________
适量的空气冶炼金属铜的化学方程式__________________________
______其中氧化剂为____________________。
(2)E的浓溶液与Cu发生反应②的化学方程式是 。
(3)利用电解可提纯粗,在该电解反应中阳极物质是 ,电解质溶液是 ;
(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿。对反应:14CuSO4+ 5FeS2 +12H2O==7Cu2S+5FeSO 4+12H2SO4
4+12H2SO4
被氧化的硫和被还原的硫的质量比为_________________________;
查看答案和解析>>
科目:高中化学 来源:2011-2012学年浙江省高三12月联考化学试卷 题型:填空题
(8分)辉铜矿(主成份为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E。G为砖红色沉淀。
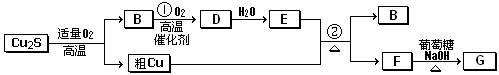
请回答下列问题:
(1)辉铜矿(Cu2S)通适量的空气冶炼金属铜的化学方程式__________________________
______其中氧化剂为____________________。
(2)E的浓溶液与Cu发生反应②的化学方程式是 。
(3)利用电解可提纯粗,在该电解反应中阳极物质是 ,电解质溶液是 ;
(4)自然界中当胆矾矿与黄铁矿(FeS2二硫化亚铁)相遇时会缓慢发生下列反应产生辉铜矿。对反应:14CuSO4+ 5FeS2 +12H2O==7Cu2S+5FeSO4+12H2SO4
被氧化的硫和被还原的硫的质量比为_________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com