
| 选项 | ① | ② | ③ | 实验结论 | 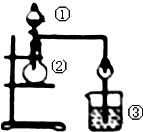 |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:C>Si |
| A、A | B、B | C、C | D、D |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
| B、溶液中导电能力的强弱主要与溶液中的离子浓度大小和离子所带电荷数有关 |
| C、强弱电解质的本质区别是溶液导电能力的强弱 |
| D、强电解质的溶液中只有离子,没有分子存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B、将少量二氧化碳通入烧碱溶液中:CO2+OH-=HCO3- |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至刚好沉淀完全:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| D、NaHCO3溶液与NaHSO4溶液混合:HCO3-+H+=H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
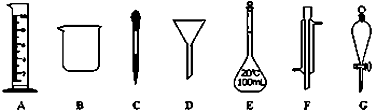
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2和Na2O2反应生成Na2CO3,推测:SO2和Na2O2反应生成Na2SO3 |
| B、金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭 |
| C、Fe3O4可表示为FeO?Fe2O3,推测:Pb3O4也可表示为PbO?Pb2O3 |
| D、F、Cl、Br,、I的单质熔点依次升高,推测N、P、As、Sb、Bi单质熔点也依次升高 |
查看答案和解析>>
科目:高中化学 来源: 题型:
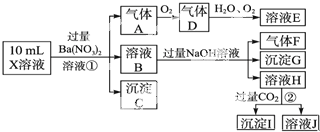
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com