
据新华社报道:从2004年5月11日16日记者发稿时为止,广州市白云区“假酒中毒”事件中的死亡人数已增加到9人,住院人数增加到33人,其中10人病危.目前广州市有关部门查明:“毒酒”窝点有5桶工业酒精,每桶工业酒精的质量为165 kg,其中甲醇的质量分数为10%.饮用甲醇5 g-15 g即可使人中毒甚至死亡.据此消息:
(1)5桶工业酒精共含甲醇________kg这些甲醇若全被酒客饮用,死亡人数将继续上升,后果不堪设想.
(2)已知工业制备甲醇的方程式为:CO+2H2=x(x即为甲醇)由此可推断甲醇的化学式为________
(3)已知甲醇的分子结构和乙醇相似,根据结构决定性质的规律,请推测甲醇的一种化学性质:________
(4)认识到掌握化学知识能帮助人们抵御有害物质的侵害,由此我们联想到误食其它有害物质使人中毒的事件还有(请举一例)________
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:山东省莱芜一中2011届高三上学期期末复习诊断性测试(二)化学试题 题型:022
据新华社报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设.可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的汽化和液化可以提高燃料的利用率.
已知25℃,101kPa时:C(s)+1/2O2(g)=CO(g) ΔH=-126.4 kJ·mol-1
2H2(g)+O2(g)=2H2O(l)
ΔH=-571.6 kJ·mol-1 H2O(g)=H2O(l) ΔH=-44 kJ·mol-1则在
25℃,101 kPa时:C(s)+H2O(g)=CO(g)+H2(g) ΔH=________.(2)
高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)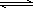 Fe(s)+CO2(g)
Fe(s)+CO2(g)
①
温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值________(填“增大”、“减小”或“不变”);②1100℃
时测得高炉中,c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,则在这种情况下,该平衡________移动(填“向左”、“向右”或“不”),判断依据是________(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g)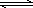 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
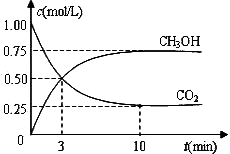
①从反应开始到平衡,氢气的平均反应速率v(H2)=________;
②下列措施能使![]() 增大的是________(填符号).
增大的是________(填符号).
A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
据新华社报道:全国农村应当在“绿色生态-美丽多彩-低碳节能-循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。可见“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的汽化和液化可以提高燃料的利用率。
已知25℃,101kPa时:C(s) +1/2O2(g)=CO(g) ΔH= -126.4 kJ·mol-1
2H2(g) +O2(g)=2H2O(l) ΔH= -571.6 kJ·mol-1 H2O(g)= H2O(l) ΔH= -44 kJ·mol-1
则在25℃,101kPa时:C(s) + H2O(g)= CO(g) + H2(g) ΔH=____________________。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
FeO(s)+CO(g) ![]() Fe(s)+CO2(g) ΔH>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) ΔH>0,已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值__________(填“增大”、“减小”或“不变”);
②1100℃时测得高炉中,c(CO2)=0.025mol·L-1,c(CO)=0.1 mol·L-1,则在这种情况下,该平衡_______移动(填“向左”、“向右”或“不”),判断依据是
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为:
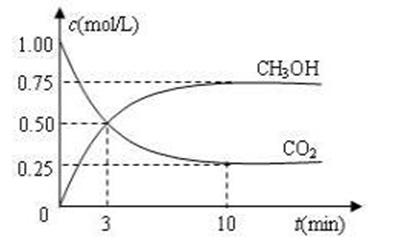
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。现向体积为1 L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。现向体积为1 L的密闭容器中,充入1mol CO2和3mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
|
 | ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
|
| |||||||||||||
| ||||||||||||||
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____________;
②下列措施能使![]() 增大的是________(填符号)。
增大的是________(填符号)。
A.升高温度 B.再充入H2 C.再充入CO2
D.将H2O(g)从体系中分离 E.充入He(g),使体系压强增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com