
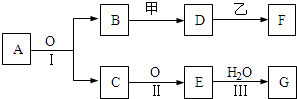
| ||
| △ |
| ||
| △ |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、氯化硼是原子晶体 |
| B、氯化硼分子是极性分子 |
| C、熔化时,氯化硼能导电 |
| D、水解方程式:BCl3+3H2O=H3BO3+3HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ CO的体积分数/% 压强/MPa | 1.0 | 2.0 | 3.0 |
| 800 | 54.0 | a | b |
| 900 | c | 75.0 | d |
| 1000 | e | f | 80.0 |
| A、b<f |
| B、900℃,2.0MPa的转化率为60% |
| C、K(1000℃)=3.2 |
| D、K(1000℃)>K(800℃) |
查看答案和解析>>
科目:高中化学 来源: 题型:
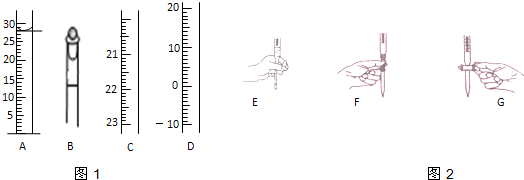
查看答案和解析>>
科目:高中化学 来源: 题型:
- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:7 | B、3:5 |
| C、1:4 | D、4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
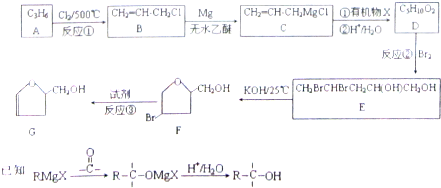
| ||
| 催化剂 |
| ||
| 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
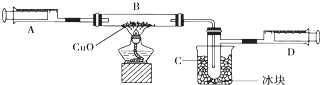
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com