
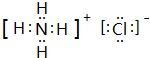 ������Һ��笠�����ˮ�⣬��Һ�����ԣ���Һ������Ũ�ȴ�СΪ��c��Cl-����c��NH4+����c��H+����c��OH-����
������Һ��笠�����ˮ�⣬��Һ�����ԣ���Һ������Ũ�ȴ�СΪ��c��Cl-����c��NH4+����c��H+����c��OH-����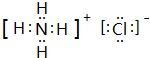 ��c��Cl-����c��NH4+����c��H+����c��OH-����
��c��Cl-����c��NH4+����c��H+����c��OH-����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��KOH Na2SO4 AlCl3 |
| B��NaCl Ba��OH��2 H2SO4 |
| C��HCl NaAlO2 NaHSO4 |
| D��Ca��OH��2 Na2CO3 BaCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1.00 mol?L-1 NaCl��Һ�к���Na+����ĿΪNA |
| B�����³�ѹ�£�6.4g�������ͳ�����ɵĻ�����к��еķ�������Ϊ0.2NA |
| C����״���£�1.12LHCHO��Cԭ�ӵ���ĿΪ0.05NA |
| D��һ��������6.4g SO2������������Ӧ����SO3��ת�Ƶ�����Ϊ0.2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����KIO3����������Һ�е�KI��5I-+IO3-+3H2O=3I2+6OH |
| B��̼��������ᷴӦ��CO32-+2H+=H2O+CO2�� |
| C��������������Һ�м����������SO32-+2H+=SO2��+H2O |
| D������������ʵ���Ũ�ȵ�����������Һ��̼�������Һ���Ba2++2OH-+NH4++HCO3-=BaCO3��+NH3?H2O+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 400�� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 X��Y��Z�����ֶ�����Ԫ�أ�X��Z��������֮����Y����������ȣ�Z�ĵ��Ӳ�����X�ĵ��Ӳ�����2����A��B��C��D��E��F����ѧ��ѧ�еij������ʣ���������������Ԫ���е�һ�֡����ֻ�������ɣ�����A����ʹʪ���ɫʯ����ֽ���������壬D��E�������ᣬEΪ��Z������������ˮ���F��һ�ֵ��ʣ���Ӧ�ܾۢ������������½��У���ת����ϵ��ͼ��ʾ��
X��Y��Z�����ֶ�����Ԫ�أ�X��Z��������֮����Y����������ȣ�Z�ĵ��Ӳ�����X�ĵ��Ӳ�����2����A��B��C��D��E��F����ѧ��ѧ�еij������ʣ���������������Ԫ���е�һ�֡����ֻ�������ɣ�����A����ʹʪ���ɫʯ����ֽ���������壬D��E�������ᣬEΪ��Z������������ˮ���F��һ�ֵ��ʣ���Ӧ�ܾۢ������������½��У���ת����ϵ��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ����֪��Ӧ���̷��ȣ����������������ֺ���Ԫ�ص����ӣ�����ClO-��ClO3-�������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ��ͼ��ʾ������˵����ȷ����
��1����һ������Cl2ͨ��һ��Ũ�ȵĿ��Լ���Һ�У�����ǡ����ȫ��Ӧ����֪��Ӧ���̷��ȣ����������������ֺ���Ԫ�ص����ӣ�����ClO-��ClO3-�������ӵ����ʵ�����n���뷴Ӧʱ�䣨t���ı仯ʾ��ͼ��ͼ��ʾ������˵����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����� | ||
| B���ٷ��Ǣڷ���2�� | ||
C���ٷ��Ǣڷ���
| ||
D���ٷ��Ǣڷ���
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com