
氮元素有着多变价态和种类繁多的化合物,因在生产、生活中发挥着重要的作用。完成下列问题:
(1)在一密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g) △H<0,其化学平衡常数K与温度T的关系如下表:
2NH3(g) △H<0,其化学平衡常数K与温度T的关系如下表:
| T | 298 K | 398 K | 498 K | … |
| K | 4.1×106 | K1 | K2 | … |
①比较K1、K2的大小:K1______K2(填“>”、“=”或“<”)。
②若保持容器的容积不变,则该反应达到化学平衡状态的依据是________(填序号)。
a.2v(H2)正=3v(NH3)逆 b.v(N2)正=3v(H2)逆
c.容器内压强保持不变 d.混合气体的平均摩尔质量保持不变
③若维持容器的压强不变,达到平衡状态后再向容器中通入一定量的N2,此时逆反应速率______(填“增大”、“减小”或“不变”);平衡常数_____。(填“增大”、“减小”或“不变”)
④已知AgCl可溶于氨水中,而AgBr不溶于氨水中,则Ksp(AgCl)____ Ksp(AgBr) (填“>”、“=”或“<”)。
( 2 )肼是氮元素的另一种氢化物,分子式为N2H4。
①298 K时,1.00 g N2H4(l)与足量的N2O4(l)完全反应生成氮气和水,放出19.15 kJ的热量。写该反应的热化学方程式_____________________________________。
②肼也可以在纯氧中燃烧生成氮气和水,为了充分利用其能量有人设计了原电池装置,电极材料是多孔石墨电极,电解质为能够传导H+的固体电解质,请写出负极反应式____________________。
科目:高中化学 来源: 题型:
A为某短周期非金属元素的单质,常用作电极材料及润滑剂。将其与铁片等如图I组装好,通电一段时间后,溶液颜色变浅,请回答:

(1)A极发生的电极反应式是___________________________________。
(2)停止通电,从图I装置中取出铁电极,用蒸馏水清洗干净后,投入盛有过量稀硫酸的烧杯中,如图Ⅱ所示。
①反应开始后的现象是________________________________。
②若使反应速率减慢,可采取的操作是__________(选填字母)。
a. 加入少量水 b. 加入少量无水CH3COONa固体 c. 通入少量HCl气体
(3)已知在强碱性环境中,Fe(OH)3可与NaClO溶液作用而生成FeO42-。
①此反应的离子方程式是____________________________,
②若反应中生成10mol水,则电子转移数是_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,现对该混合物作如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积):

回答下列问题:
(1)写出反应④的离子方程式______________________________________________。
(2)填写下表中的空白。(注:若混合物中不存在该成分,则“质量”栏中填“0”;画斜线的表格不需填写)
| 成分 | 质量 | 判断依据或计算推理过程 |
|
| ||
| (NH4)2SO4 | ||
| MgCl2 | ||
| FeCl2 | ||
| AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图,将纯Fe棒和石墨棒插入1 L饱和NaCl溶液中。下列说法正确的是( )
A.M接负极,N接正极,当两极产生气体总量为22.4 L(标准状况)时,生成
1 mol NaOH
B.M接负极,N接正极,在溶液中滴人酚酞试液,C电极周围溶液变红
C.M接负极,N接正极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段
时间后,烧杯中产生蓝色沉淀
D.M接电源正极,N接电源负极,将C电极换成Cu电极,电解质溶液换成CuSO4 溶液,则可实现在铁上镀铜
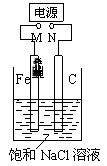
查看答案和解析>>
科目:高中化学 来源: 题型:
在溶液中,CaCl2+CO2+H2O=CaCO3↓+2HCl在任何条件下都不能发生,原因是该反应的( )
A △H >0 ΔS>0 B △H<0 ΔS<0 C △H<0 ΔS>0 D △H >0 ΔS<0
查看答案和解析>>
科目:高中化学 来源: 题型:
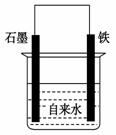
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是 ( )
A.正极的电极方程式为:O2+2H2O+4e-===4OH-
B.将石墨电极改成Mg电极,难以观察到铁锈生成
C.若向自来水中加入少量NaCl(s),可较快地看到铁锈
D.向铁电极附近吹入O2比向石墨电极附近吹入O2,铁锈出现得快
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列少量杂质(括号内杂质),简述操作步骤,并写出有关变化的离子方程式:
| 物质 | 操作步骤 | 离子方程式 |
| (1)SiO2(Al2O3) | ||
| (2)NaHCO3溶液(Na2CO3) | ||
| (3)FeCl2溶液(FeCl3) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com