
| ||
(
| ||
| (400-36.5)g |


 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
Ǧ�������ڶ��ε�أ���缫���Ϸֱ���Pb��PbO2���������ҺΪһ��Ũ�ȵ����ᣬ����ʱ���õ�ص��ܷ�ӦΪPbO2+Pb+2H2SO4=2PbSO4+2H2O��PbSO4���ܡ�
��1�������ع���ʱ�����ĵ缫��ӦʽΪ
��2����������ȵ�������ʯī���ֱ����CuSO4��Һ�У������Ӹ�����Pb����ʯī���Ӹ�����PbO2����һ��ʱ�����������ʯī��������3.2�ˣ���CuSO4��Һ���� �����ӡ����٣� �ˣ����Ҫ��CuSO4��Һ�ָ����뿪ʼʱ��ȫ��ͬ������Լ������������е�
A��CuSO4��Һ B��CuCO3���� C��CuO���� D��Cu(OH)2����
E��Cu���� F�� Cu2(OH) 2CO3����
��3�����ø���������Դ�����ö��Բ������缫�����400�˱���ʳ��ˮ��������������ĵ����Ϊ5��������Ũ�ȴ�1.5mol/L����1.3mol/Lʱ������ʣ����Һ���Ȼ��Ƶ��������������¶����Ȼ��Ƶ��ܽ��Ϊ32�ˣ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010��2011ѧ�꽭��ʡ�γ���ѧ��һ�ڶ�ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�������
Ǧ�������ڶ��ε�أ���缫���Ϸֱ���Pb��PbO2���������ҺΪһ��Ũ�ȵ����ᣬ����ʱ���õ�ص��ܷ�ӦΪPbO2+Pb+2H2SO4=2PbSO4+2H2O��PbSO4���ܡ�
��1�������ع���ʱ�����ĵ缫��ӦʽΪ
��2����������ȵ�������ʯī���ֱ����CuSO4��Һ�У������Ӹ�����Pb����ʯī���Ӹ�����PbO2����һ��ʱ�����������ʯī��������3.2�ˣ���CuSO4��Һ���� �����ӡ����٣� �ˣ����Ҫ��CuSO4��Һ�ָ����뿪ʼʱ��ȫ��ͬ������Լ������������е�
| A��CuSO4��Һ | B��CuCO3���� | C��CuO���� | D��Cu(OH)2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�갲��ʡ�����и���4���������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
Ǧ�������ڶ��ε�ء���ͼ��Ǧ���س䡢�ŵ�ʱ�Ĺ���ʾ��ͼ���������H2SO4��Һ����ط�ӦΪ��Pb+PbO2+4H++2SO42�� 2PbSO4+2H2O
2PbSO4+2H2O
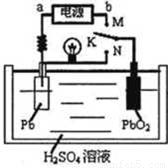
�����й�˵����ȷ����
A��ʵ������Ǧ��������Դ��ⱥ��ʳ��ˮ��ȡ���������Ƶ�����2.24L�����������ĵ�H2SO4�����ʵ����� 0.2mol
B��K��N���ʱ��H+��������Ǩ��
C��K��M����ʱ�����õ�Դ��b��Ϊ����
D��K��M���ʱ������������pH������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com