
下列热化学方程式或离子方程式中,正确的是( )
A.甲烷的标准燃烧热为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 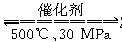 2NH3(g)
2NH3(g)
ΔH=-38.6 kJ·mol-1
C.氯化镁溶液与氨水反应:Mg2++2OH-===Mg(OH)2↓
D.氧化铝溶于NaOH溶液:Al2O3+2OH-===2AlO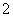 +H2O
+H2O
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
反应2SO2+O2 2SO3在密闭容器中进行。下列关于该反应的说法错误的是
2SO3在密闭容器中进行。下列关于该反应的说法错误的是
A.升高温度能加快反应速率 B.使用恰当的催化剂能加快反应速率
C.增大O2的浓度能加快反应速率 D.SO2与O2能100%转化为SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实与胶体性质无关的是
A.工业生产中常用静电除尘装置除去废气中的固体悬浮物
B.三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
C.一束平行光线照射豆浆时,可看到光亮的通路
D.万里长江流入大海处,形成长江三角洲
查看答案和解析>>
科目:高中化学 来源: 题型:
某品牌糖衣片补血剂,除去糖衣后显淡蓝绿色,主要成分是硫酸亚铁,不含其它铁的化合物。某研究性学习小组为测定该补血剂中硫酸亚铁的含量进行了以下探究:
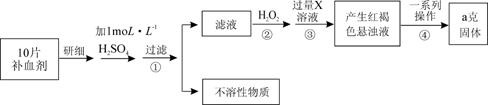
请回答下列问题:
Ⅰ.(1)实验时用10mol·L-1的浓硫酸配制100 mL 1 mol·L-1 H2SO4溶液,所需浓硫酸的体积为 mL。
(2)容量瓶所具备的功能是 (填序号)。
A.配制一定体积准确浓度的溶液 B.长期贮存溶液
C.常用来代替量筒量取一定体积的液体 D.用来溶解固体溶质
(3)在下列配制过程示意图中,错误的有(填序号) 。
 |
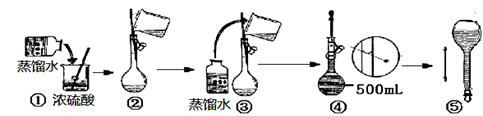
(4)下列说法正确的是 。
A.洗涤烧杯2~3次,并将洗涤液移入容量瓶以减少误差
B.某同学将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察, 所配溶液浓度会偏低
Ⅱ.(1)步骤③中产生的红褐色物质是(填化学式) 。
(2)从红褐色的悬浊液到最后的称量,其过程中所需的基本操作为:
a. , b. 洗涤, c. 灼烧, d. 冷却
(3)若称得固体的质量为ag,则每片补血剂中含硫酸亚铁的质量为 g。
查看答案和解析>>
科目:高中化学 来源: 题型:
在298 K、100 kPa时,已知:2H2O(g)===O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)===2HCl(g) ΔH2
2Cl2(g)+2H2O(g)===4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是( )
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为
2NH3(g)+NO(g)+NO2(g)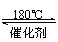
 2N2(g)+3H2O(g) ΔH<0
2N2(g)+3H2O(g) ΔH<0
在恒容的密闭容器中,下列有关说法正确的是( )
A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了A~R九种元素在周期表的位置:
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | E | R | F | |||||
| 3 | A | C | D | H | I | G | ||
| 4 | B |
(1)写出R单质分子的电子式 。
(2)A、C、D三种元素的氧化物对应的水化物中碱性最强的是 (填化学式)。
(3)A、B、C三种元素的阳离子按离子半径由大到小的顺序排列为 。
(用元素的离子符号表示)。
(4)写出A的单质与水反应的化学方程式 。
(5)X元素是A~R九种元素中的一种,X的原子核里有14个中子,2.7gX在氧气里燃烧时,质量增加2.4g。X的氢氧化物既能溶于氢氧化钠溶液中反应,也能与盐酸反应。X的元素符号是 ,它位于元素周期表中第 周期、第 族。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生成过程。
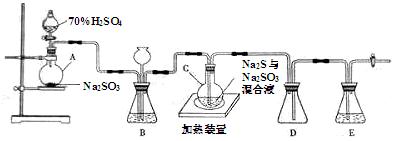
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若 ,则整个装置气密性良好。装置D的作用是 。装置E中为 溶液。
(2)装置A中反应的化学方程式为 。
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (I)
2H2S+SO2=3S+2H2O (II)
S+Na2SO3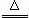 Na2S2O3 (III)
Na2S2O3 (III)
为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com