
下列说法正确的是 ( )。
A.SO2和SO3都是酸性氧化物,二者的水溶液都是强酸
B.将铜片放入浓硫酸中,无明显现象是因为铜片发生了钝化
C.硫粉在过量的纯氧中燃烧可以生成大量的SO3
D.富含硫黄的矿物在工业上可用于制造硫酸
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
某含铬Cr2O2-7废水用硫酸亚铁铵[FeSO4·(NH4)2SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n mol FeO·FeyCrxO3。不考虑处理过程中的实际损耗,下列叙述错误的是
A.消耗硫酸亚铁铵的物质的量为n(3x+l)mol
B.处理废水中Cr2O2-7的物质的量为 mo1
mo1
C.反应中发生转移的电子的物质的量为6nx mol
D.在FeO·FeyCrxO3中3x=y
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于油脂的叙述错误的是 ( )。
A.从溴水中提取溴可用植物油作萃取剂
B.用热的纯碱溶液去油污效果更好
C.硬水使肥皂去污能力减弱是因为发生了沉淀反应
D.用热的纯碱溶液可区别植物油和矿物油
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关合成洗涤剂的叙述错误的是 ( )。
A.在洗涤剂烷基苯磺酸钠中,烷基含碳原子的个数以12~18为宜
B.在洗涤剂烷基苯磺酸钠中,烷基应以带有支链的为宜
C.在合成洗涤剂中添加酶制剂可提高洗涤效果
D.在合成洗涤剂中应以无磷助剂代替含磷助剂
查看答案和解析>>
科目:高中化学 来源: 题型:
在实验探究课上,同学们积极思考,共设计出如图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是 ( )。
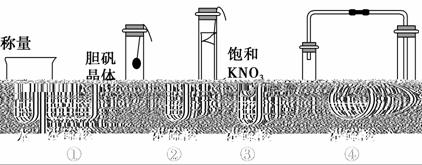
A.①②③④ B.仅①③④
C.仅①②④ D.仅②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)===Na2SO3(aq)+H2S(aq) (Ⅰ)
2H2S(aq)+SO2(g)===3S(s)+2H2O(l)(Ⅱ)
S(s)+Na2SO3(aq)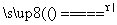 Na2S2O3(aq)(Ⅲ)
Na2S2O3(aq)(Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若________,则整个装置气密性良好。装置D的作用是_______ _______________________________________________________________。
装置E中为________溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为________。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择________。
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是____________________。已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是_____________ ___________________________________________________________。
反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有 ________。
a.烧杯 b.蒸发皿
c.试管 d.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论:
_____________________________________________________________。
已知Na2S2O3·5H2O遇酸易分解:S2O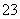 +2H+===S↓+SO2↑+H2O
+2H+===S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
据英国广播公司2013年8月27日报道,瑞典科学家发现了115号元素存在的新证据,科学家们利用某种变化(记为X)合成了115号元素。如果这一发现获得认可,元素周期表将增加“新成员”,下面有关说法中错误的是 ( )。
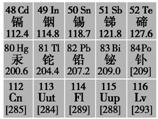
A.X变化属于一种核变化 B.该核素不能稳定存在
C.该元素的最高正价为+5价 D.该元素属于非金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com