
| A、Na2O2 |
| B、NaOH |
| C、H2O2 |
| D、H2S |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、对于N2(g)+3H2(g)?2NH3(g),缩小体积使压强增大 |
| B、对于N2(g)+3H2(g)?2NH3(g),容器体积固定不变时,充入Ar |
| C、对于N2(g)+3H2(g)?2NH3(g),容器体积固定不变时,充入N2 |
| D、对于N2(g)+3H2(g)?2NH3(g),容器气体压强不变时,充入Ar |
查看答案和解析>>
科目:高中化学 来源: 题型:


 (R可表示烃基或氢原子)
(R可表示烃基或氢原子) 的合理线路(其他无机试剂任选,用流程图表示:写出反应物、产物及主要反应条件).
的合理线路(其他无机试剂任选,用流程图表示:写出反应物、产物及主要反应条件).| Cl2 |
| 光照 |
| NaOH溶液 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第ⅠA族元素的金属性比第ⅡA族元素的金属性强 |
| B、同周期非金属氧化物对应水化物的酸性从左到右依次增强 |
| C、第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
| D、第三周期元素的离子半径从左到右逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2、H2、NH3的物质的量浓度不再改变 |
| B、nN2:nH2:nNH3=1:3:2 |
| C、N2和H2物质的量之和为NH3的2倍 |
| D、单位时间内反应1mol N2同时反应3mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
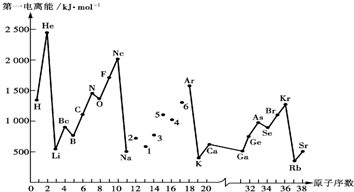
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com