

分析 木屑的主要成分是纤维素[(C6H10O5)n],酸溶后得葡萄糖溶液,用葡萄糖还原硝酸得NO和NO2,用NaOH吸收NO和NO2,得到NaNO2;HNO3不稳定,温度过高发生分解,所以反应温度不宜高于60℃,NaOH溶液呈碱性,可以用碳酸钠溶液代替,
(1)酸溶过程中,硫酸的作用是催化剂;
(2)硝酸易分解,则A装置须控制反应液的温度不高于60℃的原因是温度过高会导致硝酸的分解;反应中产生的NO2、NO被碳酸钠溶液吸收即转化为亚硝酸钠;
(3)NO和NO2的物质的量比=1:1时恰好可以看作亚硝酸,因此若(NO):n(NO2)>1:1,则会导致排放气体中NO含量升高;若n(NO):n(NO2)<1:1时NO2过量,则又会产生硝酸钠;
(4)已知NaNO2能把酸性条件下的Fe2+氧化,说明氮元素的化合价降低,同时产生一种有毒的气体,因此该气体是NO;
(5)由于NaNO2有还原性,能使酸性KMnO4溶液褪色,所以可以通过氧化还原滴定测定其纯度.
解答 解:(1)酸溶过程中,硫酸的作用是催化剂,
故答案为:催化剂或使纤维素水解成为葡萄糖;
(2)硝酸易分解,则A装置须控制反应液的温度不高于60℃的原因是温度过高会导致硝酸的分解,使NaNO2产率降低;反应中产生的NO2、NO被碳酸钠溶液吸收即转化为亚硝酸钠,
故答案为:温度过高会导致硝酸的分解,使NaNO2产率降低;b;
(3)NO和NO2的物质的量比=1:1时恰好可以看作亚硝酸,因此若(NO):n(NO2)>1:1,则会导致排放气体中NO含量升高;若n(NO):n(NO2)<1:1时NO2过量,则又会产生硝酸钠,即会使产品中混有的杂质为NaNO3,
故答案为:排放气体中NO含量升高;NaNO3;
(4)已知NaNO2能把酸性条件下的Fe2+氧化,说明氮元素的化合价降低,同时产生一种有毒的气体,因此该气体是NO,所以该反应的离子方程式为NO2-+2H++Fe2+=NO↑+Fe3++H2O,故答案为:NO2-+2H++Fe2+=NO↑+Fe3++H2O;
(5)由于NaNO2有还原性,能使酸性KMnO4溶液褪色,所以可以通过氧化还原滴定测定其纯度,因此实验方案设计为:准确称量适量的NaNO2样品放入锥形瓶中,加适量水溶解,然后用c3mol•L-1酸性KMnO4溶液滴定至溶液由无色恰好变为浅红色,且半分钟内不褪色,读数,重复以上操作2~3次,
故答案为:然后用c3mol•L-1酸性KMnO4溶液滴定至溶液由无色恰好变为浅红色,且半分钟内不褪色,读数,重复以上操作2~3次.
点评 本题考查物质制备实验方案设计与探究,为高频考点,把握制备原理、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
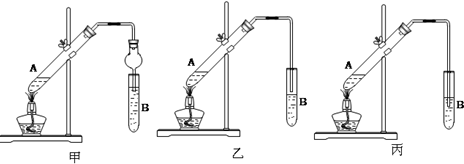
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
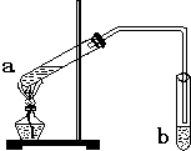 “酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用如图所示的装置制备,其中a中加乙醇、乙酸和浓硫酸,在试管b中加入7mL饱和碳酸钠溶液.连接好装置.用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
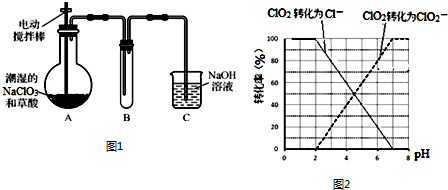
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=+244.1kJ/mol | B. | △H=-488.3kJ/mol | C. | △H=-996.6kJ/mol | D. | △H=+996.6kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
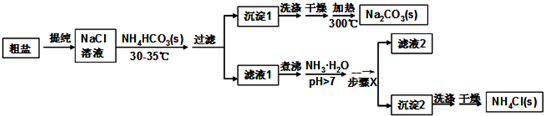
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ•mol-1) | 414 | 489 | 565 | 155 |
| A. | +1940 kJ•mol-1 | B. | -1940 kJ•mol-1 | C. | -485 kJ•mol-1 | D. | +485 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验中,乙烯的用量不会影响该反应的反应焓变△H | |
| B. | 0.5 mol H2O(l) 完全反应放出的热量为22.9 kJ | |
| C. | 1 mol C2H5OH(g)具有的能量大于1 mol C2H4(g)和1 mol H2O (g)所具有的能量和 | |
| D. | 1 mol C2H4(g)和1 mol H2O (g)中化学键的总键能大于1 mol C2H5OH(g)中化学键的总键能 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com