
某工厂的废渣中混有少量的锌粉和氧化铜(其他成分不跟酸反应),跟大量废盐酸接触形成污水,产生公害.若向污水中撒入铁粉且反应后铁粉有剩余,此时污水中一定含有的金属离子是( )
|
| A. | Fe2+、Cu2+ | B. | Cu2+、H+ | C. | Zn2+、Fe2+ | D. | Zn2+、H+ |
考点:
铁的化学性质.
专题:
几种重要的金属及其化合物.
分析:
根据氧化铜和锌粉的废渣与废盐酸混合后会生成氯化铜与氯化锌,加入铁粉由于铁的活动性比铜强所以可以置换出溶液中的铜,据此分析解答即可.
解答:
解:当少量的氧化铜和锌粉混合后氧化铜与锌都可以与盐酸反应生成氯化锌和氯化铜,且因为铁的活动性比铜强所以可以置换出氯化铜溶液中的铜而生成氯化亚铁,且由于铁粉过量,所以溶液中一定不会存在氯化铜,由于铁的活动性比锌弱所以不会置换出氯化锌溶液中的锌,所以溶液中一定含有的溶质是ZnCl2、FeCl2,
因此溶液中含有的金属离子是Zn2+、Fe2+;
故选C.
点评:
此题是对金属活动性顺序的考查,解题时可依据金属活动性顺序的意义解决.


科目:高中化学 来源: 题型:
已知碳碳单键可以绕键轴自由旋转,结构简式为: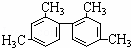 的烃,下列说法正确的是()
的烃,下列说法正确的是()
A. 分子中至少有9个碳原子处于同一平面上
B. 分子中至少有11个碳原子处于同一平面上
C. 分子中至少有16个碳原子处于同一平面上
D. 该烃属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语使用正确的是()
A. 次氯酸的结构式:H﹣Cl﹣O B. CO2的比例模型 
C. 甲基的电子式: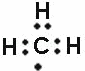 D. 漂粉精的主要成分:CaCl2
D. 漂粉精的主要成分:CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,pH=5的NH4Cl溶液中,由水电离出的OH﹣浓度是()
A. 1×10﹣5mol/L B. 1×10﹣7mol/L C. 1×10﹣9mol/L D. 1×10﹣14mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10﹣10,Ksp(AgY)=1.0×10﹣12,Ksp(AgZ)=8.7×10﹣17.
(1)根据以上信息,判断AgX、AgY、AgZ三者的溶解度(已被溶解的溶质的物质的量/1L溶液)S(AgX)、S(AgY)、S(AgZ)的大小顺序为 .
(2)若向AgY的饱和溶液中加入少量的AgX固体,则c(Y﹣) (填“增大”“减小”或“不变”).
(3)在25℃时,若取0.188g的AgY(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中Y﹣的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
配制250ml 0.10mol/L的NaOH溶液时,下列实验操作会使得配制的溶液浓度偏大的是( )
|
| A. | 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 |
|
| B. | 在容量瓶中进行定容时,仰视刻度线 |
|
| C. | 在容量瓶中进行定容时,俯视刻度线 |
|
| D. | 定容且把容量瓶倒置摇匀后,发现液面下降,又补充了水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 将固体CuO加入稀H2SO4中 CuO+2H+=Cu2++H2O |
|
| B. | 盐酸滴加在石灰石上 CaCO3+2H+=Ca2++H2CO3 |
|
| C. | Ba(OH)2溶液与稀硫酸混合 Ba2++SO42﹣=BaSO4↓ |
|
| D. | 铜片加入稀盐酸中 Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是()
A. 密度比为16:11 B. 密度比为11:16
C. 体积比为16:11 D. 原子数比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 0.1mol/L硫酸铵溶液中各离子的浓度由大到小的顺序是:c (NH4+)>c(SO42﹣)>c(H+)>c(OH﹣)
B. 在苏打与小苏打的混合溶液中存在:c(Na+)+c(H+)=c(OH ﹣)+2c(CO32﹣)+c(HCO3﹣)
C. 在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,证明Na2CO3溶液中存在水解平衡
D. 常温常压下能自发进行的反应,一定都是放热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com