
| A.熔点:NaI>NaBr | B.硬度:MgO>CaO |
| C.晶格能:NaCl<NaBr | D.熔沸点:CO2>NaCl |
科目:高中化学 来源:不详 题型:单选题
| A.简单立方堆积、配位数6、空间利用率68% |
| B.体心立方堆积、配位数6、空间利用率68% |
| C.六方最密堆积、配位数8、空间利用率74% |
| D.面心立方最密堆积、配位数12、空间利用率74% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
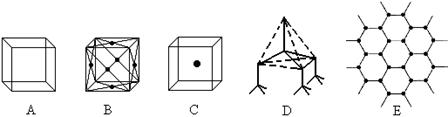
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
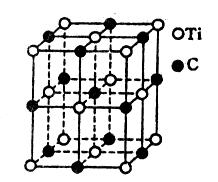
| A.TiC | B.Ti14C13 |
| C.Ti4C7 | D.Ti13C14 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 920 | 801 | 1291 | 190 | -107 | 2073 | -57 | 1723 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z的基态原子价电子排布为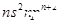 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为65,中子数为36 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
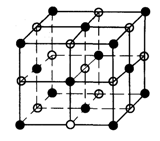
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com