
| 选项 | 实验方案 | 实验目的 |
| A | 金属甲、乙在氢氧化钠溶液中构成原电池 | 验证甲、乙的活性强弱 |
| B | 用惰性电极电解不同浓度的AgNO3和Cu(NO3)2的混合溶液 | 证明单质铜比银活泼 |
| C | 在氢氧化镁和氢氧化钠溶液中加入氯化铁溶液 | 证明Ksp[Fe(OH)3]<Ksp[Mg(OH)2] |
| D | 测定0.1mol•L-1Na2X、0.1mol•L-1Na2Y溶液的pH | 验证H2X和H2Y酸性的相对强弱 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.能与氢氧化钠反应的金属只有铝,活泼性比铝强的金属反而与氢氧化钠溶液不反应;
B.浓度不铜,不能进行比较;
C.含有氢氧化钠,加入氯化铁生成氢氧化铁沉淀,不存在难溶电解质的溶解平衡移动;
D.酸越弱,对应的钠盐水解程度越大.
解答 解:A.不能通过金属在氢氧化钠溶液失电子判断其活泼性相对较弱,如镁,铝、铁,铝,因能与氢氧化钠反应的金属只有铝,故A错误;
B.浓度不铜,不能进行比较,如硝酸铜浓度较大,则先析出铜,故B错误;
C.含有氢氧化钠,加入氯化铁生成氢氧化铁沉淀,如证明存在难溶电解质的溶解平衡移动,可在氢氧化镁浊液中滴加氯化铁,故C错误;
D.酸越弱,对应的钠盐水解程度越大,通过测定pH,可验证H2X和H2Y酸性的相对强弱,故D正确.
故选D.
点评 本题考查化学实验方案的设计,为高频考点,涉及原电池以及难溶电解质的溶解平衡、弱电解质的电离等,把握相关反应原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH3•H2O═NH4++OH- | B. | H2S?S2-+2H+ | ||
| C. | CaCO3?Ca2++CO32- | D. | CH3COONH4═CH3COO-+NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是周期表中原子序数小于20的9种元素单质的沸点与原子序数的关系,图中原子序数是连续的.试根据如图,回答下列问题:
如图是周期表中原子序数小于20的9种元素单质的沸点与原子序数的关系,图中原子序数是连续的.试根据如图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1 Na2CO3溶液中,含CO${\;}_{3}^{2-}$数目小于NA | |
| B. | 1mol FeCl3完全转化为氢氧化铁胶体后,其中胶体粒子数目为NA | |
| C. | 25℃时,1L pH=12的Ba(OH)2溶液中含有的OH-数目为0.02NA | |
| D. | 1mol苯和苯甲酸的混合物完全燃烧时消耗O2的分子数为7.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
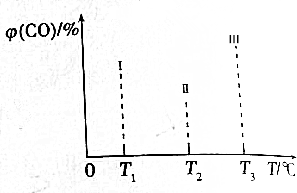
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 选项 | 现象或事实 | 解释 |
| A | 用热的纯碱溶液洗去油污 | Na2CO3可直接与油污反应 |
| B | 常温下,在足量的浓、稀硝酸中分别加入相同的铝片,浓硝酸中铝片先溶解完 | 反应物浓度越大,反应速率越快 |
| C | 用pH计、电导率仪(一种测量溶液导电能力的仪器)均可监测乙酸乙酯的水解程度 | 乙酸乙酯是非电解质,它不能导电,它的水解产物乙酸是电解质(弱酸) |
| D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含Cu2+的溶液中置换出铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验序号 | 0.1032mol/LHCl溶液体积/mL | 待测NaOH溶液体积/mL |
| 1 | 27.83 | 25.00 |
| 2 | 25.53 | 25.00 |
| 3 | 27.85 | 25.00 |
| 化学式 | AgCl | AgBr | AgI | Ag2S | Ag2CrO4 |
| 颜色 | 白色 | 浅黄色 | 黄色 | 黑色 | 红色 |
| Ksp | 1.8×10-10 | 5.0×10-13 | 8.3×10-17 | 2.0×10-48 | 1.8×10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
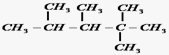
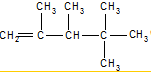 、
、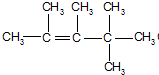 、
、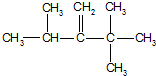 .
.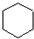 ,E是CH3CH3.
,E是CH3CH3.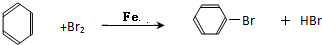 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com