
分析 Ⅰ.依据硫酸钡不溶于水和盐酸的性质解答;
Ⅱ.依据碳酸钡能够与盐酸反应生成氯化钡,氯化钡溶于水,钡离子为重金属离子能够使蛋白质变性解答;
Ⅲ.(1)含有相同的离子能抑制硫酸钡的溶解,难溶物质向更难溶物质进行转化,硫酸根离子或钡离子浓度越大,硫酸钡的溶解度越小;
(2)根据硫酸钡的溶度积常数计算硫酸根离子和钡离子浓度;
(3)先计算混合溶液中氢氧根离子浓度,再根据离子积公式计算氢离子浓度,从而确定溶液的pH值.
解答 解:Ⅰ.BaSO4既不溶于水,也不溶于酸,可经人体排出体外,不会引起Ba2+中毒,所以可以用BaSO4作为钡餐透视;
故答案为:BaSO4既不溶于水,也不溶于酸,可经人体排出体外,不会引起Ba2+中毒;
Ⅱ.碳酸钡能够与盐酸反应生成氯化钡,离子方程式:BaCO3+2H+=Ba2++H2O+CO2↑,氯化钡溶于水,钡离子为重金属离子能够使蛋白质变性,能够使人中毒;
故答案为:BaCO3遇到胃酸生成Ba2+会使人中毒,反应离子方程式为:BaCO3+2H+=Ba2++H2O+CO2↑;
Ⅲ.(1)根据难溶电解质的溶度积常数知,溶液中硫酸根离子浓度越大,硫酸钡的溶解度越小,钡离子浓度越低,氢氧化钡能抑制硫酸钡的电离,但氢氧化钡溶液中含有钡离子,所以钡离子浓度最大;水中的钡离子浓度次之;硫酸钠溶液和硫酸溶液中都含有硫酸根离子,抑制硫酸钡的电离,硫酸钠中的硫酸根浓度大于硫酸中的浓度,所以硫酸钠溶液中钡离子的浓度小于硫酸溶液中钡离子浓度,所以钡离子浓度大小顺序是:③>①>④>②;硫酸钡溶液中加入硫酸根离子和钡离子都会导致硫酸钡的沉淀溶解平衡逆移,硫酸钡的溶解度减小,硫酸根离子或钡离子浓度越大,硫酸钡的溶解度越小,所以BaSO4的溶解度的大小顺序:①>④>③>②,
故答案为:A;C;
(2)已知25℃时,Ksp(BaSO4)=1.1×10-10,上述条件下,溶液③中的c(SO42-)=$\frac{Ksp}{c(B{a}^{2}{\;}^{+})}$=$\frac{1.1×10{\;}^{-10}}{0.2}$=5.5×10-10mol/L,
②中C(Ba2+)=$\frac{1.1×10{\;}^{-10}}{0.5}$=mol/L=2.2×10-10mol/L,
故答案为:5.5×10-10mol/L,2.2×10-10mol/L;
(3)40ml 0.2mol•L-1的Ba(OH)2溶液和40ml 0.1mol•L-1的H2SO4溶液中混合后溶液中C(OH-)=$\frac{(0.2-0.1)mol/L×2×0.04L}{0.04L×2}$=0.1mol/L,则C(H+)=10-13 mol/L,所以pH=13,
故答案为:13.
点评 本题考查了沉淀溶解平衡移动影响因素,溶度积常数及溶度积规则的应用,明确沉淀溶解平衡理论是解题关键,注意溶度积规则的应用,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 两种不溶物的Ksp相差越大,不溶物就越容易转化为更难溶的不溶物 | |
| B. | 常温下,浓度均为0.1mol/L①醋酸、②盐酸、③醋酸钠溶液,水电离程度的顺序为③>①>② | |
| C. | 常温下,将相同体积的pH=3硫酸和pH=11一元碱BOH溶液混合,所得溶液可能为中性也可能为酸性 | |
| D. | 物质的浓度相同的①氯化铵溶液、②硫酸铵溶液、③碳酸氢铵溶液,pH的顺序为:③>①>② |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/K | 298 | 398 | 498 | … |
| 平衡常数(K) | 4.1×105 | K1 | K2 | … |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水中加入少量ZnSO4固体时,水的电离平衡向正反应方向移动,Kw减小 | |
| B. | 在ZnSO4溶液中各离子的浓度关系为:2c(Zn2+)+c(H+)═c(OH-)+2c(SO42-) | |
| C. | 在0.5 L 0.10 mol•L-1的ZnSO4溶液中加入等体积的0.02 mol•L-1的AgNO3溶液,即可生成Ag2SO4沉淀 | |
| D. | 常温下,要除去0.20 mol•L-1 ZnSO4溶液中的Zn2+,至少要调节pH≥8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 压强/MPa C% 速度/℃ | 0.1 | 10 | 20 |
| 200 | 15.3 | 81.5 | 86.4 |
| 300 | 2.2 | a | 64.2 |
| 400 | 0.4 | 25.1 | 38.2 |
| 500 | 0.1 | 10.6 | 19.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
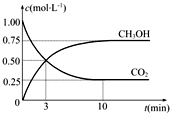 “低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO的燃烧热为283kJ | |
| B. | 25℃、101 kPa时,1 mol CO和2 mol CO的燃烧热相等 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H<-452 kJ/mol | |
| D. | CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com