

| ĪļÖŹ | ČŪµć/”ę | ·Šµć/”ę |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
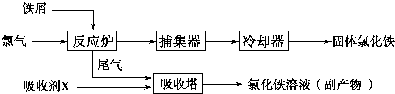
·ÖĪö ŹµŃéŹŅŅŖÓĆ»ĘĮףذ×Į×£©ÓėøÉŌļµÄCl2Ä£Äā¹¤ŅµÉś²śÖĘČ”PCl3Į÷³ĢĪŖ£ŗA×°ÖĆÅØŃĪĖįŗĶ¶žŃõ»ÆĆĢ¶žÕß·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£¬ÖʵĆĀČĘų£¬ŅņPCl3ÓöĖ®»įĒæĮŅĖ®½ā£¬ĖłŅŌĀČĘųŠčøÉŌļ£¬B×°ÖĆĄūÓĆÅØĮņĖįøÉŌļĀČĘų£¬ĄūÓƶžŃõ»ÆĢ¼Åž”×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹»ĘĮףذ×Į×£©×ŌČ¼£¬PCl3·ŠµćĪŖ75.5”ę£¬ĄūÓĆE×°ÖĆ·ĄÖ¹PCl3»Ó·¢£ØĄäÄż£©£¬ŅņĪ²ĘųÖŠŗ¬ÓŠÓŠ¶¾ĘųĢåĀČĘų£¬ĒŅæÕĘųÖŠĖ®ÕōĘųæÉÄܽųČė×°ÖĆ£¬ĖłŅŌÓĆF×°ÖĆĄūÓĆ¼īŹÆ»ŅĪüŹÕ¶ąÓąµÄCl2£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČėÉÕĘæŗĶPCl3·“Ó¦£¬
£Ø1£©A×°ÖĆÖŠ¶žŃõ»ÆĆĢŗĶÅØŃĪĖį·“Ó¦ÖĘČ”ĀČĘų£¬¾Ż“ĖŹéŠ“Ąė×Ó·“Ó¦·½³ĢŹ½£»
£Ø2£©ĀČĘųĪŖĖįŠŌĘųĢ壬ŠčÓĆĖįŠŌøÉŌļ¼ĮøÉŌļ£¬¼īŹÆ»ŅĪüŹÕ¶ąÓąĀČĘų·ĄÖ¹ĪŪČ¾æÕĘų£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČėÓ°Ļģ²śĘ·“æ¶Č£»
£Ø3£©°×Į×ÄÜ×ŌČ¼£¬ĶØČė¶žŃõ»ÆĢ¼øĻ¾»æÕĘų£»
£Ø4£©ŅĄ¾ŻĪļÖŹµÄ·ŠµćŹżÖµ²»Ķ¬£¬æÉŅŌĄūÓĆÕōĮóµÄ·½·Ø·ÖĄė³öČżĀČ»ÆĮ×£»
£Ø5£©ĒāŃõ»ÆÄĘÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆÄĘŗĶ“ĪĀČĖįÄĘ£»
£Ø6£©ŅĄ¾Ż·“Ó¦µÄ»Æѧ·½³ĢŹ½H3PO3+H2O+I2=H3PO4+2HI”¢I2+2Na2S2O3=2NaI+Na2S4O6 æÉÖŖn£ØH3PO3£©=n£ØI2£©×Ü-n£ØNa2S2O3£©”Į$\frac{1}{2}$£¬25mLČÜŅŗÖŠH3PO3µÄĪļÖŹµÄĮæµČÓŚČżĀČ»ÆĮ×µÄĪļÖŹµÄĮ棬ŌŁĒó³öČżĀČ»ÆĮ×µÄ×ÜĪļÖŹµÄĮæŗĶÖŹĮæ£¬Č»ŗóĒó³öÖŹĮæ·ÖŹż£®
½ā“š ½ā£ŗŹµŃéŹŅŅŖÓĆ»ĘĮףذ×Į×£©ÓėøÉŌļµÄCl2Ä£Äā¹¤ŅµÉś²śÖĘČ”PCl3Į÷³ĢĪŖ£ŗA×°ÖĆÅØŃĪĖįŗĶ¶žŃõ»ÆĆĢ¶žÕß·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£¬ÖʵĆĀČĘų£¬ŅņPCl3ÓöĖ®»įĒæĮŅĖ®½ā£¬ĖłŅŌĀČĘųŠčøÉŌļ£¬B×°ÖĆĄūÓĆÅØĮņĖįøÉŌļĀČĘų£¬K3ĄūÓƶžŃõ»ÆĢ¼Åž”×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹»ĘĮףذ×Į×£©×ŌČ¼£¬PCl3·ŠµćĪŖ75.5”ę£¬ĄūÓĆE×°ÖĆ·ĄÖ¹PCl3»Ó·¢£ØĄäÄż£©£¬ŅņĪ²ĘųÖŠŗ¬ÓŠÓŠ¶¾ĘųĢåĀČĘų£¬ĒŅæÕĘųÖŠĖ®ÕōĘųæÉÄܽųČė×°ÖĆ£¬ĖłŅŌÓĆF×°ÖĆĄūÓĆ¼īŹÆ»ŅĪüŹÕ¶ąÓąµÄCl2£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČėÉÕĘæŗĶPCl3·“Ó¦£¬
£Ø1£©A×°ÖĆÖŠ£¬¼ÓČČĢõ¼žĻĀ£¬ÅØŃĪĖįŗĶ¶žŃõ»ÆĆĢ¶žÕß·“Ӧɜ³ÉĀČ»ÆĆĢ”¢ĀČĘųŗĶĖ®£¬Ąė×Ó·½³ĢŹ½ĪŖMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£¬
¹Ź“š°øĪŖ£ŗMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£»
£Ø2£©ŅņPCl3ÓöĖ®»įĒæĮŅĖ®½ā£¬ĖłŅŌĀČĘųŠčøÉŌļ£¬ĀČĘųŗĶÅØĮņĖį²»·“Ó¦£¬ĖłŅŌÄÜÓĆÅØĮņĖįøÉŌļĀČĘų£¬ŅņĪ²ĘųÖŠŗ¬ÓŠÓŠ¶¾ĘųĢåĀČĘų£¬ĒŅæÕĘųÖŠĖ®ÕōĘųæÉÄܽųČė×°ÖĆ£¬ĖłŅŌÓĆF×°ÖĆĄūÓĆ¼īŹÆ»ŅĪüŹÕ¶ąÓąµÄCl2£¬·ĄÖ¹æÕĘųÖŠµÄĖ®ÕōĘų½ųČėÉÕĘæŗĶPCl3·“Ó¦£¬
¹Ź“š°øĪŖ£ŗÅØĮņĖį£»ĪüŹÕ¶ąÓąµÄĀČĘų”¢·ĄÖ¹æÕĘųÖŠµÄH2O½ųČėÉÕĘæŗĶPCl3 ·“Ó¦£»
£Ø3£©ĶØČėŅ»¶ĪŹ±¼äµÄCO2æÉŅŌÅž”×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹°×Į×ÓėæÕĘųÖŠµÄŃõĘų·¢Éś×ŌČ¼£¬¹Ź“š°øĪŖ£ŗÅž”×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹°×Į××ŌČ¼£»
£Ø4£©ÓÉŠÅĻ¢æÉÖŖ£¬POCl3ÓėPCl3¶¼ŹĒŅŗĢ壬·ŠµćĻą²ī½Ļ“󣬹ŹæÉŅŌÓĆÕōĮóµÄ·½·Ø½ųŠŠ·ÖĄė£¬¹Ź“š°øĪŖ£ŗÕōĮó£»
£Ø5£©ĒāŃõ»ÆÄĘÓėĀČĘų·“Ӧɜ³ÉĀČ»ÆÄĘŗĶ“ĪĀČĖįÄĘ£ŗCl2+2OH-=Cl-+ClO-+2H2O£¬¹Ź“š°øĪŖ£ŗCl2+2OH-=Cl-+ClO-+2H2O£»
£Ø6£©0.1000mol•L-1µāČÜŅŗ10.00mLÖŠŗ¬ÓŠµāµ„ÖŹµÄĪļÖŹµÄĮæĪŖ£ŗ0.1000mol•L-1”Į0.0100L=0.00100mol£¬øł¾Ż·“Ó¦I2+2Na2S2O3=2NaI+Na2S4O6æÉÖŖ£¬ÓėĮ×Ėį·“Ó¦Ļūŗĵĵāµ„ÖŹµÄĪļÖŹµÄĮæĪŖ£ŗ0.00100mol-0.1000mol•L-1”Į0.00084L”Į$\frac{1}{2}$=0.00058mol£¬ŌŁÓÉH3PO3+H2O+I2=H3PO4+2HIæÉÖŖ£¬25mLČżĀČ»ÆĮ×Ė®½āŗóµÄČÜŅŗÖŠŗ¬ÓŠµÄH3PO3µÄĪļÖŹµÄĮæĪŖ£ŗn£ØH3PO3£©=n£ØI2£©=0.00058mol£¬250mLøĆČÜŅŗÖŠŗ¬ÓŠH3PO3µÄĪļÖŹµÄĮæĪŖ£ŗ0.00058mol”Į$\frac{250mL}{25mL}$=0.0058mol£¬ĖłŅŌ1.00g²śĘ·ÖŠŗ¬ÓŠµÄČżĀČ»ÆĮ×µÄĪļÖŹµÄĮæĪŖ0.0058mol£¬øĆ²śĘ·ÖŠPCl3µÄÖŹĮæ·ÖŹżĪŖ£ŗ$\frac{137.5g/mol”Į0.0058mol}{1g}$”Į100%=79.75%£¬
¹Ź“š°øĪŖ£ŗ79.75%£®
µćĘĄ ±¾Ģāæ¼²éŌĶĮ»ńČ”ŠÅĻ¢µÄÄÜĮ¦”¢¶ŌŹµŃéŌĄķĄķ½āµČ£¬ĢāÄæÄŃ¶Č½Ļ“ó£¬ŹĒ¶ŌÖŖŹ¶µÄ×ŪŗĻŌĖÓĆ£¬Ąķ½āŹµŃéŌĄķŹĒ½āĢāµÄ¹Ų¼ü£¬ŠčŅŖѧɜ¾ßÓŠŌśŹµµÄ»ł“”Óė×ŪŗĻŌĖÓĆ·ÖĪö½ā¾öĪŹĢāµÄÄÜĮ¦£¬×¢ŅāĢāÖŠŠÅĻ¢PCl3ÓöO2»įÉś³ÉPOCl3£¬POCl3ČÜÓŚPCl3£¬PCl3ÓöĖ®»įĒæĮŅĖ®½āÉś³ÉH3PO3ŗĶHCl£®


 ¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø »īĮ¦ŹŌ¾ķĻµĮŠ“š°ø
»īĮ¦ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ±ź×¼×“æöĻĀ£¬22.4LŃĪĖįŗ¬ÓŠNAøöHCl·Ö×Ó | |
| B£® | 1.0 L 1.0 mol•L-1 µÄNaAl02Ė®ČÜŅŗÖŠŗ¬ÓŠµÄŃõŌ×ÓŹżĪŖ2 NA? | |
| C£® | ³£ĪĀ³£Ń¹ĻĀ£¬14gÓÉN2ÓėCO×é³ÉµÄ»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżÄæĪŖNA | |
| D£® | ŅŃÖŖC2H4ŗĶC3H6»ģŗĻĪļµÄÖŹĮæĪŖag£¬Ėłŗ¬Ō×Ó×ÜŹżĪŖ$\frac{a{N}_{A}}{14}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
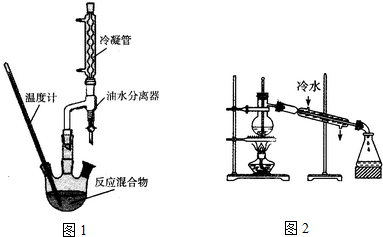
| Ļą¶Ō·Ö×ÓĮæ | ĆÜ¶Č£Øg/cm3£© | ·Šµć£Ø”ę£© | Ė®ČÜŠŌ | |
| 2-ōĒ»ł-4-±½»ł¶”Ėį | 180 | 1.219 | 357 | Ī¢ČÜ |
| ŅŅ “¼ | 46 | 0.789 | 78.4 | Ņ×ČÜ |
| 2-ōĒ»ł-4-±½»ł¶”ĖįŅŅõ„ | 208 | 1.075 | 212 | ÄŃČÜ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com