

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| ||

| 16(d+w-c) |
| c-d |
| 16(d+w-c) |
| c-d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
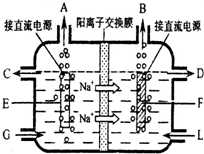 �Ĵ�ʢ�����Σ��ɾ�����ȡ��ʳ�����ճ��������Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ�
�Ĵ�ʢ�����Σ��ɾ�����ȡ��ʳ�����ճ��������Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ�2- 4 |
| �����Լ� |
| ���� |
| �������� |
| �������ᾧ����� |
2- 4 |
| ||
| ||
| ||
��V1-
|
| ||
��V1-
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com