
���� A��B��C��D����Ԫ�ؾ�Ϊ������Ԫ�أ�A���ʳ�����Ϊ����ɫ���壬����������ˮ��ɱ����������AΪCl��BԪ�ص�ԭ�Ӻ���ֻ��1�����ӣ���BΪHԪ�أ�C��DԪ�ؾ�����ͬ������������������ͬ���壬DԪ��ԭ�ӵ�K�㡢M�������֮�͵���L�������������M�������Ϊ8-2=6����DΪSԪ�ء�CΪOԪ�أ�
��� �⣺��1��A��B��C��D����Ԫ�ؾ�Ϊ������Ԫ�أ�A���ʳ�����Ϊ����ɫ���壬����������ˮ��ɱ����������AΪCl��BԪ�ص�ԭ�Ӻ���ֻ��1�����ӣ���BΪHԪ�أ�C��DԪ�ؾ�����ͬ������������������ͬ���壬DԪ��ԭ�ӵ�K�㡢M�������֮�͵���L�������������M�������Ϊ8-2=6����DΪSԪ�ء�CΪOԪ�أ�
�ʴ�Ϊ��Cl��H��O��S��
��2��AΪCl��Ԫ����Ԫ�����ڱ��е�λ�ã��������ڵڢ�A�壬������ͨ����B��C�γɵ�һ�ֻ������У���Ӧ��ɵõ�����Ư���ԵĻ���Ӧ��������ˮ��Ӧ����HCl��HClO����Ӧ����ʽΪ��Cl2+H2O=HCl+HClO��
�ʴ�Ϊ���������ڵڢ�A�壻Cl2+H2O=HCl+HClO��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��Ƚϻ�����ּ�ڿ���ѧ���Ի���֪ʶ�Ĺ��̣�


 ���ɿ��õ�Ԫ����AB��ϵ�д�
���ɿ��õ�Ԫ����AB��ϵ�д� С�����ϵ�д�
С�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
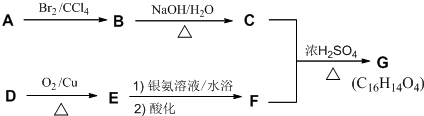
 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4����ҺpH�Ĵ�С˳�٣��ܣ��ۣ��� | |
| B�� | �١��ڻ�Ϻ�pH��7��������Һ��c��NH4+����c��NH3•H2O�� | |
| C�� | �١����зֱ����25mL0.1mol•L-1�������Һ��c��NH4+�����٣��� | |
| D�� | �ۡ����зֱ����12.5mL0.1mol•L-1NaOH��Һ������Һ������������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
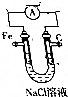 �����ʻ�úȼ���ǵ�����Դȼ�����õ���ѷ�ʽ֮һ�����������к������϶࣬ȼ�չ��̵���γɽ����Ȼ����NaCl����Cl2�����ʣ��Խ���¯����ɸ�ʴ��
�����ʻ�úȼ���ǵ�����Դȼ�����õ���ѷ�ʽ֮һ�����������к������϶࣬ȼ�չ��̵���γɽ����Ȼ����NaCl����Cl2�����ʣ��Խ���¯����ɸ�ʴ��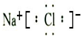 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ���� | c��HA��/mol•L-1 | c��NaOH��/mol•L-1 | ��Ӧ����ҺpH |
| �� | 0.1 | 0.1 | 9 |
| �� | c1 | 0.2 | 7 |
| A�� | �ף���Ӧ����Һ�� c��Na+����c��A-����c��OH-����c��H+�� | |
| B�� | �ң���Ӧ����Һ�� c��Na+��=c��HA��+c��A-�� | |
| C�� | ������ˮ���������c��H+��=1��10-9 mol•L-1 | |
| D�� | ����c1һ������0.2 mol•L-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 5 | B�� | 3 | C�� | 2 | D�� | 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com